Алифатические углеводороды. Типы растворителей.
Такие вещества как растворители регулярно применяются и в быту и в промышленности. Они обязательно потребуются в процессе ремонтных работ в доме, а о крупных производственных предприятиях нечего и говорить, проведение некоторых процессов просто не возможно без применения растворителей.
Что такое растворитель и каково его назначение
Растворитель - это быстроиспаряющееся жидкое химическое вещество или смесь нескольких веществ, имеющих органическую природу, обладающее способностью растворять вязкие органические субстанции, образовывая при этом однородную смесь.
В основном растворитель предназначен для лакокрасочных покрытий, а именно для доведения их до необходимой консистенции перед использованием. Некоторыми красителями невозможно воспользоваться без растворителя, например, имеющими высокую концентрацию и хранящимися в специальной таре.

Качественный растворитель, исходя из своего предназначения, должен соответствовать следующим требованиям:
- легко смешиваться с краской до однородного состояния;
- после нанесения красителя или лака растворитель должен быстро улетучиваться;
- смешиваясь с концентратом красителя растворитель не должен начинать реагировать с ними;
- свойства растворителя не должны меняться при соприкосновении с водой.
В двух словах назначение растворителя можно охарактеризовать следующим образом: обеспечение удобства нанесения красителя на поверхность и дальнейшее быстрое и незаметное исчезновение. Еще их применяют перед началом работ по покраске, обезжиривая рабочие поверхности, а так же по их завершении, очищая инструмент.
Каждое наименование в линейке лакокрасочных покрытий требует применения определенного вида растворителя. Соблюдать соответствие растворителя типу краски необходимо для того, чтобы добиться образования однородного вещества, которое не будет распадаться на составные части, и сделает возможным его распределение на требуемую площадь.
Виды растворителей
Растворители подразделяются на два вида:
- органические;
- неорганические.

Органические растворители являются наиболее востребованными, по сравнению с неорганическими, и согласно своим физическим особенностям, бывают следующих видов:
- трудноулетучивающиеся, например скипидар. Они применимы для эмалей и лаков;
- среднеулетучивающиеся, например керосин. Чаще всего они используются для масляных и акриловых красителей;
- легкоулетучивающиеся, например бензин, уайт-спирит, сольвент. Их применяют для эмалей, лаков, акриловых и масляных красителей. Взаимодействуя с данной группой растворителей необходимо быть предельно внимательным и соблюдать осторожность т.к. легкоулетучивающиеся вещества чрезвычайно взрывоопасны.
Чаще всего они являются подвижными жидкими субстанциями, со свойственным им сильным запахом, который является одним из основных недостатков.
В перечень неорганических растворителей входят:
- вода;
- жидкий аммиак;
- серные, фосфорные и др. соли.

Органические растворители, в отличие от неорганических, имеют ряд серьезных минусов, в числе которых устойчивый запах, неослабевающий на протяжении довольно долгого времени и легковоспламеняющиеся токсичные испарения, которые к тому же могут привести к серьезному отравлению.
Но, к сожалению, красители, растворяемые водой, более востребованные за рубежом, в нашей стране пока не пользуются большим спросом из-за потери качества при хранении в условиях жесткого российского климата.
Обзор растворителей наиболее часто используемых в нашей стране, их свойства
Органические растворители, несмотря на свои отнюдь не безопасные свойства, в России применяются довольно широко, чего нельзя сказать об их неорганических собратьях. Растворители делятся на три группы:
- углеводородные;
- спиртовые;
- сложные эфиры.
Ниже мы рассмотрим особенности и свойства самых распространенных из них. К углеводородным растворителям относятся:
- Уайт-спирит является маслянистой жидкостью, не имеющей цвета. Он чрезвычайно горюч и обладает запахом схожим с керосиновым. Его растворяющие показатели не слишком высоки, но, вопреки всему, уайт-спирит все же востребован из-за относительной дешевизны и нетоксичности.
- Нефтяной бензол. Жидкость, не имеющая цвета, быстро испаряющаяся, не являющаяся водорастворимой. Ей так же присущ сильный запах, как и всем веществам органической группы. Нефтяной бензол совместим с углеводородными соединениями. Выделяет токсичные, огнеопасные пары, при соприкосновении с воздухом становится взрывоопасен.
- Скипидар. Подразделяется на живичный и пневый. Живичный является лучшим. Это бледно-желтая, резко пахнущая жидкость, используемая для разведения шпатлевок и масляных лакокрасочных материалов.
- Бензин. Продукт переработки нефти, обладает огнеопасными свойствами, легко испаряется. При достижении определенного количества паров в воздухе может сдетонировать.

К спиртовым растворителям относятся следующие:
- Этиловый спирт. Он жидкий, не имеет цвета, но зато обладает узнаваемым запахом. В нем не должны присутствовать различные посторонние частицы. Его пары способны вызвать тяжелейшее отравление при условии попадания большого их количества в дыхательные пути. Он не только легко воспламеняется при контакте с огнем или искрой, но и может загореться просто при воздействии больших температур.
- Бутиловый спирт. Применяется в качестве разбавителя для нитроцеллюлозных лаков. Покрытие приобретает блеск, становится более гладким, а так же становится менее подверженным побелению.
- Метиловый спирт (метанол). Прозрачная, жидкая субстанция, обычно содержащая примесь эфиров и ацетона. Является крайне ядовитым.
- Этилетиленгликоль. Прозрачная, вязкая жидкость, не имеющая запаха. Образует однородное соединение с водой. Долго испаряется, что делает ее незаменимой при работе с нитролаками, покрытие из которых получается блестящим, гладким, легко поддающимся полировке.
Сложные эфиры представлены следующей группой растворителей:
- Метилацетат. Быстроиспаряющаяся, жидкая, подвижная субстанция, обладающая пожароопасными и ядовитыми свойствами. Закипает при температуре 56-58 градусов.
- Этилацетат. Испаряется не так быстро, закипает при температуре 77-82 градуса, обладает приятным запахом.
- Бутилацетат. Жидкий, имеет желтоватый оттенок, испаряется долго и потому используется, в случае если нужно увеличить время высыхания покрытия.
- Амилацетат. Прозрачный, жидкий, имеет приятный запах, испаряется медленно. Так же как и бутилацетат используется для замедления высыхания.
- Ацетон. Имеет характерный и очень неприятный запах, чрезвычайно летуч и пожароопасен.
- Смеси растворителей. Чтобы развести концентрированные нитролаки до нужной степени вязкости используют смеси растворителей из группы сложных эфиров. При этом качественные свойства покрытия напрямую зависит от элементов состава. Например, если в нем содержится наибольшее количество быстроиспаряющихся растворителей, то покрытие может помутнеть, но если составить смесь из веществ, замедляющих время сушки, то покрытие выйдет блестящим, гладким, незамутненным.
Обзор номерных растворителей
Растворителей существует такое огромное множество, что для того, чтобы их различать, некоторым из них стали присваивать номера, которые дают возможность ориентироваться в наименованиях и осуществлять выбор. Рассмотрим наиболее часто встречающиеся из них:
- Широкое применение получил растворитель 4 (Р-4). На самом деле он является смесью, в составе которой присутствует ацетон и толуол. В основном Р-4 используют для алкидных лаков и красок, а так же эмалей на базе хлорированных полимеров. Компоненты, присутствующие в составе растворителя, подобраны так, чтобы оказывать положительное влияние на консистенцию и формирование покрытия пленкообразующих веществ.
При необходимости его можно использовать и для обезжиривания поверхности перед нанесением покрытия, но если есть возможность лучше для этого взять другой растворитель т.к. Р-4 чрезвычайно летуч.

Он является огнеопасным, при работе с ним нужно соблюдать осторожность и использовать индивидуальные защитные средства.
- Еще более популярным является растворитель 646, незаменимый и в быту, и в промышленности. Он применим и для растворения и в качестве обезжиривателя, используется во множестве сфер, в том числе и в авторемонтных мастерских. Растворитель 646 имеет замечательные качественные характеристики. Он включает в себя целый перечень таких составляющих, за счет которых становится многофункциональным, может растворять множество разных химических соединений.
Растворитель 646 имеет желтоватый оттенок и резкий запах, быстро испаряется. В его составе присутствуют ароматические углеводороды, кетоны, спирты, эфиры. В процессе его использования нужно быть предельно аккуратным т.к. из-за его большой активности легко испортить предыдущие слои красителя. Иногда из-за этого свойства растворитель 646 даже заменяют на более слабые.
Без него невозможно изготовление и применение множества наименований лакокрасочных материалов. Растворитель 646 либо используют во время производства данной продукции, либо перед использованием разводят до нужной консистенции. Так же он незаменим при разведении некоторых шпатлевок.
Краска, разбавленная 646-м растворителем, по высыхании становится блестящей и гладкой. Эмалевые и лаковые покрытия, в которых он использовался, при нанесении легко и скоро схватываются, образовывая пленку. Когда растворитель 646 испаряется, запах исчезает.
Еще одним преимуществом, благодаря которому потребителям полюбился этот растворитель - цена, которая при всех его положительных характеристиках является довольно низкой, а так же наличие в свободном доступе - купить растворитель 646 можно в каждом строительном супермаркете.
- Так же хорошие свойства имеет растворитель 2 (РС-2). Он является прозрачной жидкостью, имеющей бледно-желтый оттенок. Быстро испаряется. В его составе присутствуют ксилол и уайт-спирит. Им растворяют масляные лаки, битумные краски, пентафталевые эмали. Испускает крайне ядовитые испарения. Работая с РС-2 необходимо всегда защищать кожу и дыхательные пути и глаза. Так же пары пагубно воздействуют на нервную систему, внутренние органы, кровь и костный мозг, попадая в организм не только через дыхательные пути, но и через кожу.
Кроме внутреннего влияния вещество может оказывать и внешнее, например, взывать сыпь при долгом соприкосновении.
Вещество огнеопасно, при накоплении паров в воздухе может произойти взрыв.
Области использования растворителей
Как уже было отмечено выше, растворитель для краски необходим для следующих работ:
- разведение загустевших или высококонцентрированных эмалевых и лакокрасочных материалов;
- чистка предметов или одежды выпачканной краской;
- очистка инструмента использованного при нанесении лакокрасочных покрытий.
Растворители используют во многих областях. Для каждого вида она своя. Например, ацетон с успехом задействуют в процессе синтезирования поликарбонатов, эпоксидных смол и полиуретанов. Растворяют с его помощью масла, природные смолы, полиакрилаты, хлоркаучук, а так же жиры, воски, резину.
Уайт-спирит применим для любых лакокрасочных материалов. Подходит для масляных красок, лаков, эмалей, грунтовок, автомобильных мастик. Им обезжиривают поверхности, очищают инструмент.

Керосин, бензин и прочие углеводороды служат для растворения жиров, масел, парафина, восков.
Растворители, относящиеся к группе эфиров, например этилацетат, бутилацетат, растворяют полярные синтетические смолы, церризин.
Растворители из группы спиртов, этил, бутил, метил и прочие, используют для производства лаков, а так же для растворения полиэфирных смол и нитроцеллюлозы.
Правила работы с растворителями
Почти все органические растворители оказывают действие той или иной степени тяжести на здоровье человека, в зависимости от вида. Чтобы, работая с ними не пострадать от токсичных испарений, необходимо строго соблюдать технику безопасности:
- использовать во время работ индивидуальные средства защиты, такие как перчатки, респиратор, защитные очки и т.д.;
- при попадании вещества на кожу следует его немедленно смыть, пока оно не успело подействовать или оказало минимальное воздействие;
- обеспечить доступ в помещение достаточного количества свежего воздуха;

- необходимо контролировать температуру в помещении, т.к. некоторые растворители при соприкосновении с теплым воздухом становятся взрывоопасными;
- так же следует учитывать горючесть и огнеопасность данных веществ, недопустимо проведение работ вблизи открытого огня, так же опасно курение или просто наличие поблизости горячих предметов;
- хранить растворители нужно в прохладном помещении, в небольших бутылках или канистрах, на которых обязательно должны быть этикетки;
- вся тара должна находиться пробками вверх, недопустимо ее лежание на боку или вниз пробкой.
Статья посвящена различным аспектам использования растворителей в технологических процессах изготовления электронной техники и не только.
Общие сведения
Растворители - индивидуальные химические соединения или их смеси, способные переводить различные вещества в раствор. В свою очередь, растворы - это гомогенные однородные системы, состоящие из двух или более компонентов, состав которых в определенных пределах может непрерывно изменяться . Преобладающий компонент называется растворителем, остальные - растворенными веществами. Различают газовые, жидкие и твердые растворы. К газовым относится воздух, горючие природные газы и др. На практике нам часто приходится иметь дело с жидкими растворами.
Обычно растворители применяются в качестве среды для проведения химических реакций или для технологических целей. Образование растворов существенно изменяет условия протекания химических реакций между компонентами. Причем многие процессы могут происходить только в растворах. Растворители создают гомогенную среду, обеспечивая контакт между реагирующими частицами (ионами, молекулами), а также влияют на механизм химических реакций, их скорость, установление равновесия и т. п. В экзотермических реакциях растворители, разбавляя реагирующие вещества, помогают отвести избыточное тепло. Как технологическое средство растворители широко применяются в различных областях техники (при производстве лаков и красок, взрывчатых веществ, в фармацевтике, парфюмерии, сельском хозяйстве и др.). Растворители находят широкое применение и в большей части микро- и макротехнологий, используемых при производстве электронной техники.
Как и все химические соединения, растворители разделяют на неорганические и органические. Важнейший неорганический растворитель - вода. Менее известные неорганические растворители - легкоплавкие галогениды (например, BrF3), оксогалогениды (например, сульфурилхлорид, тионилхлорид), азотсодержащие растворители (жидкий аммиак) и др. Круг органических растворителей гораздо шире.
Растворители можно классифицировать по их физическим свойствам.
Растворители с температурой кипения ниже 100 °С относят к низкокипящим, с температурой кипения выше 150 °С - к высококипящим.
По степени летучести растворители подразделяют на легколетучие, среднелетучие и труднолетучие.
В зависимости от величины вязкости растворители подразделяют на маловязкие (менее 2 мПа-с), средней вязкости (2-10 мПа-с) и высоковязкие (более 10 мПа-с).
В соответствии с наличием/отсутствием диполь-ного момента и величиной диэлектрической проницаемости различают полярные и неполярные растворители. В зависимости от диэлектрической проницаемости и донорно-акцепторных свойств различают четыре группы растворителей.
1. Протонные растворители (вода, спирты, карбо-новые кислоты и др.). Они являются донорами протонов и обладают высокой диэлектрической проницаемостью (ε > 15).
2. Апротонные биполярные растворители (некоторые апротонные амиды, кетоны, сульфоксиды). Обладают высокой диэлектрической проницаемостью, но не обладают донорно-акцепторными свойствами.
3. Электронодонорные растворители (эфиры).
4. Неполярные растворители с низкой диэлектрической проницаемостью (ε < 15). Это сероуглерод, углеводороды. Такие растворители не обладают донорно-акцепторными свойствами ни по отношению к протонам, ни по отношению к электронам.
В зависимости от кислотно-основных свойств, растворители могут быть кислотными (уксусная кислота), основными (пиридин), нейтральными (бензол).
Вариантов классификации растворителей великое множество, так же, как и для любых химических соединений.
Чудесная молекула
Не задумываясь, можно сказать, что самым распространенным растворителем на Земле является вода. Иногда даже говорят, что нашу планету правильнее было бы назвать Вода. Причина проста: вода занимает около 70% поверхности земного шара. Количество воды на Земле оценивается в 1,39Т0 18 т . Ученые, чтобы доказать, что в том или ином уголке Вселенной возможна жизнь (органическая жизнь), ищут там следы воды. И находят! Молекулы воды обнаружены в межзвездном пространстве. Вода входит в состав комет, большинства планет солнечной системы. Какая же она, эта удивительная, чудесная и в какой-то степени незаменимая молекула?
Так называемая брутто-формула воды (Н 2 0) известна даже двоечнику. Стереометрия, а точнее, планиметрия этой молекулы приведена ниже.
Л. Салем в книге «Чудесная молекула» использует сравнение молекулы воды с персиком, к которому прикреплены два абрикоса. Персик, расположенный в центре, - это атом кислорода. Два маленьких абрикоса по бокам - атомы водорода. Атомы водорода и кислорода расположены в углах равнобедренного треугольника. Для оценки величины молекулы воды достаточно привести длину связи О-Н. Она равна 0,0957 нм.
Поскольку атомы водорода и кислорода имеют различную электроотрицательность, а химические связи О-Н расположены под углом, отличным от 180° (104,5°), молекула воды полярна (диполь). Кроме того, она еще и поляризуема. Эти свойства во многом определяют поведение воды при взаимодействии с другими химическими соединениями.
Вода обладает очень большой диэлектрической проницаемостью. При комнатной температуре ε = 78,3. Абсолютно чистая вода - довольно хороший изолятор: удельное объемное сопротивление изоляции воды при 0°С составляет 1,47-10 б Ом-м, при 50 °С - 18,9· 10 -6 Ом-м. Можно было бы даже сказать, отличный изолятор, но этому мешает то, что незначительная доля молекул воды (примерно 1 из 5-10 -9) подвергается электролитической диссоциации по схеме:
![]()
Концентрация ионов Н + (фактически Н 3 0 +) и связанная с ней концентрация ионов ОН + характеризуются водородным показателем (рН среды). На практике на характеристику проводимости воды гораздо больше влияют растворенные в ней соли, кислоты, основания - постоянные спутники не идеально чистой, а реальной воды. Даже небольшой концентрации этих компонентов вполне достаточно для того, чтобы вода, словно по мановению волшебной палочки, превратилась из диэлектрика в проводник.
Вода - химическое соединение, без упоминания о котором невозможно объяснение смысла таких понятий, как гидрофильность и гидрофобность. Гидрофильность и гидро-фобность - характеристики взаимодействия вещества и воды. Если вещество и вода близки по строению друг к другу и сильно взаимодействуют друг с другом, например образуют водородные связи, то говорят о ги-дрофильности. При слабом взаимодействии вещества и воды говорят о гидрофобности. Мерой интенсивности межмолекулярного взаимодействия служит поверхностное натяжение на границе между веществом и водой. Молекулы воды, обладая большим диполь-ным моментом, сильно взаимодействуют и друг с другом с образованием водородных связей. Даже в водяном паре при невысоких температурах и умеренных давлениях имеется около 1% димеров воды.
Вода - прекрасный растворитель. Она хорошо растворяет полярные и диссоциирующие на ионы вещества. С точки зрения реакционной способности вода довольно инертное вещество. Но некоторые вещества, растворяясь в воде, реагируют с нею. Так, газы ΝΗ 3 и S0 2 , растворяясь в воде, превращаются в ионы NH 4 + и S0 3 2+ .
Органические растворители
Вода - самый распространенный неорганический растворитель. А вот в среде органических растворителей претендентов на лидирующее положение нет. Можно лишь выделить группу так называемых нефтяных растворителей, которых с недавних пор стали сокращенно называть нефрасами. В качестве нефтяных растворителей используются узкие прямогонные фракции или фракции, выделенные из продуктов вторичной переработки нефти.
Большинство растворителей нефтяного происхождения имеют исторически сложившиеся названия, которые часто абсолютно не связаны с их составом и химической природой соединений, входящих в их состав. В некоторых случаях названия таких растворителей не только не информируют, но даже дезинформируют пользователей об их составе. Реальный пример - уайт-спирит. Необремененные знанием английского языка так и норовят исправить «ошибку» и назвать его «уайт-спиртом». В какой-то степени они правы. Действительно, в дословном переводе с английского языка white spirit означает «белый спирт». Но такое название, видимо, отражает лишь внешнюю схожесть. Химический состав уайт-спирита очень широк: предельные углеводороды, нафтеновые углеводороды, в небольшом количестве ароматические соединения и др. А вот спиртовая составляющая, увы, отсутствует.
В стремлении упорядочить и унифицировать названия растворителей нефтяного происхождения и появилось название нефрасы. По углеводородному составу нефрасы разделяют на следующие типы:
- нефрасы С - растворители смешанного состава, в которых присутствуют углеводороды всех классов;
- нефрасы А - растворители с преобладанием алифатических углеводородов и пониженным содержанием ароматических углеводородов (не более 2,5%);
- нефрасы И - растворители с преобладанием изопарафиновых углеводородов;
- нефрасы П - растворители с преобладанием парафиновых углеводородов;
- нефрасы Н - растворители с преобладанием нафтеновых углеводородов;
- нефрасы Ар - растворители с преобладанием ароматических углеводородов.
Поскольку нефрасы не являются индивидуальными растворителями, для них не характерна фиксированная температура кипения. Они выкипают в определенном диапазоне температур. Этот диапазон также указывается в их названии.
Так, например, сольвент в соответствии с такой классификацией называется А 130/150. Это означает, что сольвент представляет собой смесь углеводородов с преобладанием алифатических и пониженным содержанием ароматических соединений, выкипающую в диапазоне температур от 130 до 150 °С.
В условном обозначении широко используемых в производстве электронной техники бензинов-растворителей БР-1 (СЗ 80/120) и БР-2 (С2 80/120) присутствует еще одна цифра. Дело в том, что группа растворителей смешанного типа (С) в зависимости от содержания ароматических соединений подразделяется на подгруппы:
- 0 - менее 0,1%;
- 1 -от 0,1% до 0,5%;
- 2 - от 0,5% до 2,5%;
- 3 - от 2,5% до 5,0%;
- 4 - от 5,0% до 25,0%;
- 5 - от 25,0% до 50,0%.
Говорят, что бензины БР-1 и БР-2 взаимозаменяемы. Действительно, фракционный состав у них близок. Но если эти растворители используются для отмывки или обезжиривания чего-либо, излишне чувствительного к активным растворителям, предпочтение следует отдать последнему. Он содержит меньше ароматических углеводородов. Кроме того, он менее токсичен. Если же избирательность не является главным требованием к растворителю, то ответ, очевидно, будет иным.
Аналогичные мысли возникают по отношению к уайт-спириту. Отечественный растворитель содержит гораздо больше ароматических соединений, нежели его зарубежный аналог (до 16%). Очищенный от ароматических соединений уайт-спирит почти не имеет запаха, но его растворяющая способность значительно меньше.
В отличие от нефтяных растворителей, индивидуальные органические растворители характеризуются константами своих физических свойств. Хотя для технических растворителей также характерен некоторый диапазон, в пределах которого изменяются эти свойства. Но этот диапазон гораздо меньше, чем у нефтяных растворителей. Растворителями богаты практически все известные классы органических соединений: предельные углеводороды; хлорированные углеводороды; ароматические соединения; спирты; простые и сложные эфиры; кетоны и др. Физические свойства некоторых наиболее распространенных органических растворителей приведены в таблице 1.
Термодинамика растворов
Растворы низкомолекулярных и/или высокомолекулярных соединений являются обратимыми системами. Они подчиняются правилу фаз Гиббса и могут быть описаны обычными диаграммами состояния.
Растворение является самопроизвольным процессом и сопровождается уменьшением изобарно-изотермического потенциала (ΔG):
где ΔН - изменение теплосодержания (энтальпии) системы, ΔS - изменение энтропии системы, Т - абсолютная температура, р - давление.
Растворимость химических соединений в растворителях определяется термодинамическим сродством, мерой которого является разность изобарно-изотермических потенциалов раствора и суммы изобарно-изотермических потенциалов компонентов:
Чем больше по абсолютной величине ΔG смеси, тем больше сродство между компонентами, тем лучше растворимость.
Если же уйти от уравнений, то можно сказать, что при растворении главенствует принцип «подобное растворяется в подобном». Максимальное значение ΔG смеси будет в том случае, если растворяемое вещество и растворитель будут максимально похожи друг на друга. Общее правило: гидрофильные вещества лучше растворяются в гидрофильных растворителях, а гидрофобные -в гидрофобных. Поэтому попытки растворить обойный клей в бензине всегда будут обречены на неудачу. Термодинамика выступает против этого.
Гидрофильно-гидрофобный баланс
Однажды ко мне обратился знакомый технолог, озадаченный нелогичным, на его взгляд, поведением меламино-алкидного лака. Нелогичность выражалась в том, что нужно было уменьшить его вязкость, а он не желал растворяться. На вопрос о том, чем вы его пытались растворить, ответ был такой: «Тем, чем рекомендовано на этикетке - уайт-спиритом». Как сделать так, чтобы лак не захотел растворяться в том, в чем он обязан растворяться? Для решения задачи не нужно изобретать ничего нового. Решение уже есть, нужно попытаться виртуально его повторить, ограничивая себя лишь тем, что можно использовать только внутренние ресурсы системы.
На вопрос, что вы делали с этим лаком, был получен ответ: «Лак использовался ранее для пропитки трансформаторов». Пребывание трансформаторов в лаке, скорее всего, не могло привести к таким «тяжелым» последствиям. После уточнения вопроса оказалось, что речь шла о вакуумной пропитке трансформаторов. На этой стадии причина столь неожиданного явления мне была ясна уже на 90%. А после того, как я посмотрел, какие растворители используются в лаке изначально, 90% уже превратились в 100%.
В молекулах полимерного (олигомерного) связующего меламино-алкидных лаков имеются как гидрофобные, так и гидрофильные фрагменты. Поэтому в этих лаках используется смесь растворителей (уайт-спирит или его аналоги и бутанол). Первый отвечает за растворение гидрофобных фрагментов связующего, а второй - за растворение гидрофильных.
В нормальных условиях испаряется преимущественно более летучий растворитель. В данном случае - уайт-спирит или его аналоги. Поэтому изготовители и рекомендуют при загустевании лака разводить его уайт-спиритом. Но если лак подвергается воздействию вакуума, то улетучивается еще и менее летучий растворитель - бутанол. И добавления только уайт-спирита уже недостаточно, чтобы растворить загустевший лак. Гидрофильные группировки связующего лака просят еще и близкого им по химической природе растворителя.
Обобщая, можно сказать, что полимеры или олигомеры (связующие большей части лакокрасочных материалов) содержат в своих молекулярных цепочках гидрофобные и гидрофильные фрагменты. За гидрофобные свойства ответственны метильные, этильные и другие углеводородные радикалы. Гидроксильные, карбоксильные и другие полярные группировки гидрофильны. Поэтому растворители также должны включать компоненты с преимущественно гидрофобными свойствами (уайт-спирит, толуол, сольвент и т. п.) и компоненты, имеющие сродство к воде (этанол, этилцеллозольв, ацетон, этилацетат и др.). А их сочетание определяется химической природой связующего лака. Для получения некоторых лаков набор универсальных «номерных» растворителей (таблица 2) недостаточен. Поэтому приходится изобретать собственные неповторимые комбинации компонентов растворителя. Гидрофильно-гидрофобный баланс может быть реализован и в пределах молекул одного растворителя.
Аналогичные проблемы встречаются в технологиях отмывки печатных узлов от загрязнений. В общем случае последние также отличаются по своей полярности и, соответственно, гидрофильности/гидро-фобности. В известной спирто-бензиновой смеси первая составляющая отвечает за растворение гидрофильных загрязнителей (в первую очередь остатков канифоли), а вторая - за растворение гидрофобных загрязнителей (жиры и т. д.). В изопропи-ловом спирте (основе многих отмывочных жидкостей зарубежного производства) гидрофильно-гидрофобный баланс реализуется преимущественно в пределах одной молекулы.
Растворы полимеров
Растворы полимеров и их низкомолекулярных аналогов (олигомеров) будут интересны преимущественно специалистам, занимающимся нанесением полимерных покрытий и герметизацией радиоэлектронной аппаратуры полимерными материалами.
Таблица 1. Физические свойства некоторых индивидуальных органических растворителей
Таблица 2. Рецептура некоторых «номерных» растворителей и разбавителей
Растворы полимеров обладают целым рядом особенностей по сравнению с растворами низкомолекулярных соединений из-за специфических свойств макромолекул: больших размеров, широкого диапазона гибкости, большого набора конформаций (пространственных конфигураций), способности изменять конформаций при изменении температуры или смене растворителя и т. д. Растворы полимеров характеризуются высокой вязкостью, замедленной диффузией, обладают тиксотропией и т. д. Все это, с одной стороны, осложняет работу с ними, а с другой - предоставляет гораздо больше потенциальных возможностей.
Особенностью процесса растворения высокомолекулярных соединений является их набухание. Скорость диффузии макромолекул значительно меньше, чем скорость диффузии молекул растворителя. Поэтому последние быстрее проникают в полимерную фазу, чем макромолекулы в растворитель. В результате объем полимера сильно увеличивается. Набухание не всегда может закончиться растворением. Если полимер и растворитель смешиваются друг с другом ограниченно, в конце процесса образуется две фазы: насыщенный раствор полимера в растворителе и насыщенный раствор растворителя в полимере. С изменением условий, например температуры, ограниченное растворение может перейти в неограниченное, и наоборот.
Полимеры пространственного (трехмерного) строения в лучшем случае могут только набухать. Наличие химических связей не позволяет макромолекулам оторваться друг от друга и перейти в раствор.
На практике при приготовлении растворов полимеров учитывают специфику их растворения, не вводя в раствор сразу весь растворитель. В противном случае на поверхности полимера образуется набухшая оболочка, препятствующая дальнейшему проникновению растворителя. С такой проблемой, думаю, сталкивались те, кто пытался за один прием приготовить обойные клеи на основе крахмала, карбоксиметилцеллюлозы и прочих водорастворимых полимеров.
Фазовое равновесие в системе «полимер - растворитель» устанавливается правилом фаз Гиббса:
где С - число степеней свободы в системе, К - число компонентов, Ф - число фаз.
Правило фаз определяет состояние системы в момент равновесия, независимо от пути, по которому система подошла к этому состоянию. Число степеней свободы С указывает, сколько переменных, определяющих состояние системы, можно произвольно изменять, не изменяя числа фаз.
Из этого уравнения следует, что в двухкомпонентных системах максимальное число степеней свободы равно трем. Это означает, что состояние системы «полимер - растворитель» полностью определяется температурой, давлением и концентрацией полимера. Поскольку в конденсированных системах равновесие почти не зависит от давления, поэтому правило фаз можно записать в упрощенном виде:
Однофазная система имеет две степени свободы. При наличии двух фаз система имеет всего одну степень свободы. Это означает, что изменение температуры автоматически приводит к изменению концентрации в обеих фазах.
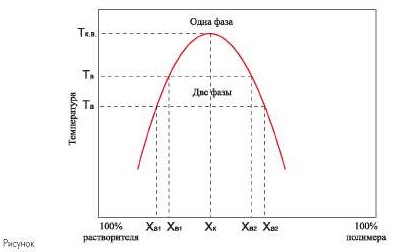
На рисунке приведена типичная кривая фазового равновесия в двухкомпонентной системе «полимер - растворитель».
Кривая фазового равновесия отделяет область неограниченного растворения от области ограниченного растворения.
В области ограниченного растворения, например в точке «а», число фаз равно 2, а число степеней свободы - 1. Состояние системы однозначно определяется либо температурой, либо концентрацией. В точке «а» раствор полимера характеризуется температурой Т а и составом фаз: фаза 1 - х a1 и фаза 2 - х a2 . При повышении температуры концентрации растворов в обеих фазах начинают сближаться, изменяются и объемы фаз. При достижении температуры Т кв (верхней критической) составы обеих фаз выравниваются, и происходит переход из двухфазной системы в однофазную - гомогенный раствор полимера в растворителе. Охлаждение однофазной системы вновь приведет к расслоению. Такой переход может быть осуществлен неограниченное количество раз.
Фазовые диаграммы для реальных систем «полимер - растворитель» не так просты. Отсутствует резкая граница между областями неограниченного и ограниченного растворения. Вследствие полидисперсности полимеров кривая фазового равновесия практически представляет набор кривых, отвечающих отдельным фракциям полимера. Фазовое расслоение в растворах полимеров может происходить не только при понижении, но и при повышении температуры.
В отличие от растворов низкомолекулярных соединений, растворы полимеров даже при очень небольших концентрациях представляют собой довольно вязкие среды. Но главное отличие не в этом. Способность молекул полимеров деформироваться под действием внешнего силового поля и ориентироваться в потоке приводит к тому, что вязкость становится переменной величиной.
Течение низкомолекулярных жидкостей и их растворов подчиняется закону Ньютона:
где τ - напряжение сдвига, Па; η - коэффициент вязкости, Па•с; γ - скорость сдвига (градиент скорости сдвига), с -1 .
В ньютоновских жидкостях вязкость η не зависит от напряжения (скорости) сдвига. В структурированных системах в большинстве случаев вязкость зависит от напряжения сдвига. Растворы полимеров в общем случае являются неньютоновскими жидкостями. Их вязкость уменьшается с увеличением градиента скорости. Чем быстрее течет такая жидкость, тем меньше ее вязкость. Объяснение очень простое. В области низких концентраций отдельные макромолекулы ориентируются вдоль потока. В области высоких концентраций разрушаются структуры, возникающие при взаимодействии макромолекул друг с другом. При очень малых или при очень больших скоростях потока растворы полимеров также подчиняются закону Ньютона.
Эффективная вязкость растворов полимеров зависит от концентрации, молекулярной массы полимера, его молекулярно-массового распределения, температуры и природы растворителя.
Известны различные виды вязкости: кинематическая, динамическая, относительная, удельная, приведенная, а для полимеров еще и характеристическая. Характеристическая вязкость - это приведенная вязкость, экстраполированная к нулевой концентрации полимера.
На практике о вязкости полимеров чаще всего судят, измеряя не абсолютные значения, а время истечения жидкости через калиброванное отверстие. В лакокрасочном производстве технологи обычно оперируют так называемой вязкостью по ВЗ-4 . Измерение такой вязкости сводится к измерению времени истечения (в секундах) определенного объема лакокрасочного материала из обыкновенной воронки через калиброванное отверстие. Поскольку технология нанесения лакокрасочных покрытий допускает изменение вязкости в довольно широком интервале, точность такого измерения бывает вполне достаточной. Для высоковязких лакокрасочных материалов используют воронки с подогревом.
Более точные измерения проводят при тер-мостатировании на капиллярном вискозиметре, например ВПЖ-1, ВПЖ-2, ВПЖ-4 . При этом появляется возможность перейти от секунд к абсолютным значениям вязкости.
Растворы наоборот
Большинство практически используемых полимеров в чистом виде не обладают высокоэластическими свойствами. Такие свойства могут у них появиться при добавлении специальных низкомолекулярных соединений,
называемых пластификаторами . Система «полимер - пластификатор», по сути дела, представляет собой очень концентрированный раствор, в котором содержание пластификатора изменяется в диапазоне от долей процента до десятков процентов. Это своеобразные растворы с обратным знаком - раствор жидкости в твердом веществе (твердый раствор).
Пластифицировать можно практически все полимеры. Для обеспечения необходимого комплекса эксплуатационных свойств система «полимер - пластификатор» должна в течение длительного времени сохранять свои свойства. Это достигается использованием в качестве пластификаторов веществ, имеющих высокую температуру кипения и очень низкую летучесть.
Пластификаторы классифицируют по химической природе и степени совместимости с полимером. Впервые в качестве пластификатора была использована камфора, а первой пластифицируемой пластмассой был целлулоид (Англия, 2-я половина XIX века). Сейчас в качестве пластификаторов наибольшее распространение получили сложные эфиры фталевой кислоты (примерно 80% всего объема). Применяются также эфиры алифатических дикарбоновых кислот, эфиры фосфорной кислоты, низкомолекулярные полиэфиры, хлорированные парафины, кремнийорганические жидкости, парафины, продукты лесохимического производства и др.
Сущность пластификации заключается в увеличении гибкости и подвижности макромолекул в присутствии низкомолекулярного компонента. Как правило, непременным условием пластификации является термодинамическая совместимость пластификатора с полимером, то есть образование истинного раствора пластификатора в полимере. При использовании пластификатора, имеющего термодинамическое сродство к полимеру, происходит самопроизвольное образование его истинного раствора в полимере (полимер набухает в пластификаторе).
Если пластификатор не имеет сродства к полимеру, его введение в полимер можно осуществить принудительно - в смесителях. В этом случае образуется термодинамически неустойчивая коллоидная система, склонная к расслаиванию. Внешне это проявляется в появлении капелек пластификатора на поверхности изделия. При удачном сочетании «полимер - пластификатор» такие процессы происходят с очень медленной скоростью, вследствие чего изделия сохраняют эксплуатационные свойства в течение нескольких десятков лет.
По характеру взаимодействия с полимерами пластификаторы могут быть разделены на две группы: полярные и неполярные. Первые способны сольватировать полярные группы полимера, снижая их межмолекулярное взаимодействие и, следовательно, температуру стеклования. Понижение температуры стеклования при этом пропорционально числу молей введенного пластификатора (правило Журкова). Неполярные пластификаторы существенно не изменяют внутреннюю энергию системы. Они играют роль своеобразной смазки. Поэтому иначе их называют мягчителями.
Особый вид пластификации - пластификация полимера полимером. Эластичность жесткого полимера можно увеличить добавлением к нему эластичного полимера. Обязательное условие - термодинамическое сродство полимеров. Пример такой термодинамически устойчивой системы: «по-ливинилхлорид - бутадиеннитрильный каучук».
Водные устремления
Есть химические соединения, называемые изоцианатами . Изоцианаты содержат функциональные группировки -NCO. Это чрезвычайно химически активные и к тому же токсичные соединения. Высокая химическая активность и высокая токсичность, как правило, соседствуют друг с другом. В производстве электронной техники изоцианаты находят применение в качестве отвердителя алкидно-уретанового лака УР-231 - диэти-ленгликольуретан (ДГУ), при изготовлении компаундов и др.
Высокая химическая активность изоциа-натов находит практическое применение и в иных областях. Так, для модификации полиолефинов диизоцианатами было синтезировано химическое соединение с очень длинным названием: 1,1-1,6-гексаметилен-3,3,3 1 ,3 1 -тетракис-(2-оксиэтил)-бисмочеви-на (далее - бисмочевина). Добавку получали в результате взаимодействия 1,6-гек-саметилендиизоцианата и диэтаноламина по реакции:
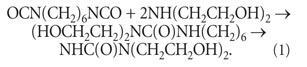
Эта добавка случайно оказалась в руках медиков. Оказалось, что она обладает уникальными криопротекторными свойствами. Еще из школьного курса физики мы знаем, что в отличие от большинства химических соединений, вода при замерзании не уменьшается в объеме, а увеличивается. Именно благодаря этому лед не тонет, а плавает. Именно благодаря этому сохраняется жизнь в водоемах и т. д. С другой стороны, благодаря этому же свойству воды при замерзании любого живого существа кристаллики льда необратимо разрушают органические клетки. Но биообъекты (кровь, костный мозг, человеческие органы и др.) можно длительно сохранять, замораживая их при температуре жидкого азота (-196 °С) в присутствии криопротекторов. На практике для этого чаще всего используется ди-метилсульфоксид, довольно токсичное и недостаточно эффективное соединение. Оказалось, что бисмочевина обладает прекрасными криопротекторными свойствами. И самое главное, несмотря на чрезвычайную токсичность используемых для ее получения химических соединений, сама она практически нетоксична. По словам разработчиков, ее можно даже намазывать на хлеб и есть его.
Вслед за положительными результатами испытаний возникла потребность в разработке промышленной технологии получения бисмочевины. Первоначально синтез добавки проводился по реакции (1) с использованием традиционной для химии технологии - в среде органического растворителя. Целевой продукт получался в виде раствора и выделялся в кристаллическом виде известными методами, например многократной перекристаллизацией. Технология сложна и многостадийна, особенно на стадии очистки бисмочевины от примесей. Химики обычно, если имеется возможность, стремятся уйти от органических растворителей. И разработчики ушли от них, заменив органический растворитель на обычную воду. Решение сверхоригинальное. Дело в том, что исходный продукт (диизоцианат) активно реагирует с водой. Было предложено проводить реакцию при очень низкой (отрицательной) температуре. При такой температуре реакция (1) еще идет, а скорость реакции диизоцианата с водой практически снижается до нуля. Выбирая это решение, разработчики имели в виду, что даже при нормальной температуре скорость реакции (1) была в несколько раз выше скорости реакции диизоцианата с водой. Целевой продукт получался в виде водного раствора, именно в таком виде он и использовался в медицине. Следовательно, необходимость в выделении бисмочевины из раствора отпадала. В теории, а в некоторых случаях и на практике, все получалось прекрасно. Но почему-то водный раствор бисмочевины, полученный по этой технологии, часто оказывался токсичным.
Автор присоединился к разработчикам технологии на этой стадии. Отдавая должное красоте технического решения, можно сказать, что оно было не лишено недостатков. Принципиальный недостаток технологии заключался в том, что она была работоспособна лишь тогда, когда исходные продукты в реакции (1) взяты в абсолютно стехиометрических соотношениях. Теоретически это возможно, а практически мы можем только более или менее приблизиться к этому. Напомню, что в 1 г-моле вещества содержится 6,02· 10 23 молекул (число Аво-гадро). Попробуйте ввести в реакцию вещества с такой точностью, чтобы каждой молекуле одного вещества точно отвечало столько же молекул другого вещества (в данном случае соотношение 2:1). Вряд ли это удастся. Поэтому в тех случаях, когда соотношение исходных компонентов в реакции было близко к стехиометрическому, получали нетоксичный продукт. В иных ситуациях, а они по теории вероятности должны были случаться гораздо чаще, раствор получался токсичным из-за остатков токсичных исходных соединений.
Для решения этой, казалось бы нерешае-мой, проблемы был использован известный из теории решения изобретательских задач (ТРИЗ) прием разрешения технических противоречий (использовать частично избыточное или частично недостающее действие) . Одного вещества из исходных (диизоцианат) взяли чуть больше, чем это нужно по реакции. Формула изобретения , в котором реализовано это решение, выглядит следующим образом:
Способ получения 1,1-1,6-гексаметилен-3,3,3 1 ,3 1 -тетракис-(2-оксиэтил)-бисмочевины взаимодействием 1,6-гексаметилендиизоциа-ната с диэтаноламином в среде растворителя с последующей выдержкой реакционной массы и выделением целевого продукта, отличающийся тем, что гексаметилендиизо-цианат берут в количестве 1,0005-1,1 от сте-хиометрического, а в качестве растворителя используют воду и реакционную смесь выдерживают при 25-60 °С в течение времени, необходимого для выработки 1,6-гексамети-лендиизоцианата.
Избыточное по отношению к стехиометрическому количество 1,6-гесаметилендии-зоцианата гарантирует во всех случаях отсутствие в водном растворе целевого продукта диэтаноламина. Оставшийся в реакционной среде 1,6-гексаметилендиизоцианат при последующей выдержке в результате реакции с растворителем (водой) переводится в полимочевины. Полимочевины выпадают в осадок и отфильтровываются. Таким образом получается водный раствор бисмочевины, готовый к использованию по назначению. Инъекции такого раствора мышки, на которых проверяли его токсичность, переносили безболезненно. Таким оригинальным способом были практически реализованы «водные устремления» в этой технологии.
«Водные устремления» прослеживаются практически во всех технологиях производства электронной техники. В некоторых технологиях (нанесение гальванических или химических покрытий, травление и др.) для их реализации не требуется никаких усилий. В принципе, для получения таких покрытий можно использовать и неводные среды. Научные исследования в данном направлении ведутся. Но нужно ли это?
В других технологиях, к примеру, при формировании промежуточных или финишных покрытий печатных плат (фоторезисты, паяльные маски), чтобы уйти от органопрояв-ляемых композиций к водо-щелочепроявляе-мым, пришлось приложить немалые усилия.
Тенденция ухода от «органики» главенствует и в технологиях отмывки печатных узлов от всевозможных видов загрязнений. На смену токсичным и недружественным по отношению к окружающей среде органическим растворителям приходят моющие составы на водной основе.
Продолжение следует.
Литература
- Политехнический словарь / Редкол.: А. Ю. Ишлинский и др. М.: Сов. Энцикл. 1989.
- Химическая энциклопедия: В 5 т. Т. 1 / Редкол.: И. Л. Кнунянц и др. М.: Сов. Энцикл., 1988.
- Салем Л. Чудесная молекула // Пер. с франц. М: Мир, 1982.
- ГОСТ 8420-74. Материалы лакокрасочные. Методы определения условной вязкости.
- Мусакин А. П., Рачинский Ф. Ю., Суглобо-ва К. Д. Оборудование для химических лабораторий. Л.: Химия, 1982.
- Барштейн Р. С, Кирилович В. П., Носовский Ю. Е. Пластификаторы для полимерных материалов. М.: Химия, 1982.
- Саундерс Дж. X., Фриш К. К. Химия полиуретанов // Пер. с англ. М.: Химия, 1972.
- Пат. РФ № 2072352. Уразаев В. Г., Архиреев В. П., Батдалов Ю. Р. Способ получения ^-^б-гексаметилен-ЗДЗ^З`-тетра-кис (2-оксиэтил)-бисмочевины. Приоритет от 10.08.1994.
Растворители органического происхождения широко востребованы в химической промышленности, а также в сферах строительства, ремонта, производства ЛКМ, автомобилестроения, полиграфии и др. Их применяют для расщепления жиров, приготовления клеевых составов и пропиток, удаления загрязнений и наслоений. В статье речь пойдет о разнообразии и правильном использовании органических растворителей.
Органические растворители
Особенностью веществ является их органическая природа и способность растворять соединения различных типов. По способу их получения выделяют такие основные группы, как:
- углеводороды;
- кетоны;
- простые и сложные эфиры;
- спирты;
- галогенсодержащие растворители.
Плотности органических растворителей зависит от температуры.
Растворитель органических веществ фото

Использование органических растворителей
- Растворяющие жидкости и их гомологи широко применяются во многих промышленных сферах. Также они востребованы при восстановительных и реставрационных работах художественных ценностей. Их используют для приготовления пропиток, лаков и очищения предметов из любых материалов.
- На автомобильных предприятиях и в ремонтных цехах в основном в ход идет бензин, ксилол, хлорированные углеводороды, уайт-спирит и керосин. С их помощью осуществляется промывка, отмочка, мойка и обезжиривание машинных деталей.

Производство лакокрасочных материалов невозможно представить без органических растворителей, которые по большей части являются основой для изготовления ряда продукции.
В быту растворители необходимы в следующих случаях:
- для разбавления высококонцентрированных ЛКМ до необходимой консистенции, вязкости;
- для удаления с одежды или поверхностей пятен от красящих материалов;
- для чистки рабочего инструмента, который использовался в малярных работах (кисть, краскопульт, валик и т.д.).
Эффективное очищение наслоений или загрязнений зависит от грамотного подбора подходящего растворителя. Наиболее распространенные примеры по удалению наплывов разного характера указаны в таблице ниже.
Растворитель или разбавитель
- Многие люди используют эти слова в качестве синонимов. Однако химический состав органических растворителей обладает совершенно разными физико-техническими характеристиками. Добавление разбавителя в концентрированные материалы не предполагает протекания каких-либо реакций.
- Растворитель, в свою очередь, наоборот, воздействует на вещество, проникая в его структуру, растворяет пленкообразующие компоненты. Таким образом, краски, лаки эмали приобретают оптимальную текучесть (вязкость) для окрашивания.

Используемые растворители должны отвечать 2-м основным требованиям:
- способность преобразовывать пленкообразующие вещества в жидкое состояние;
- при испарении обеспечивать оптимальную структуру покрытия, без потери первоначальных свойств и без образования дефектов на окрашиваемой поверхности.
Виды органических растворителей
Органические растворители являются чаще жидкими веществами с характерным острым запахом. Классификация проводится по химическому строению, физическим свойствам и другим параметрам, определяющим их способность взаимодействия с различными веществами.
По составу:
- однородные составы - это бутиловый спирт, ацетон, сольвент, бензин, изопропанол;
- многокомпонентные (комбинированные) вещества - Р646, 649, Р-4 и др.
По скорости испарения:
- вещества с низкой летучестью (скипидар) применяются для эмалей и лаков;
- растворители со средней летучестью (керосин) используются в качестве разбавителей масляных красок;
- высоко летучие органические растворители (бензин, уайт-спирит) подойдут практически для всех видов лакокрасочной продукции.
Следует помнить, что чем больше степень летучести, тем выше их взрывоопасность и воспламеняемость.
По точке кипения:
- низкокипящие - до 100 градусов;
- среднекипящие - до 150 градусов;
- высококипящие - свыше 150 градусов.
По работе с органическими растворителями
В зависимости от типа растворителя, а именно его густоты, нанесение может осуществляться следующими способами:
- кистевой метод;

- окунание;
- струйный облив;
- выдержка в парах вещества;
- пневматическое, безвоздушное или электростатическое распыление;
- электроосаждение.
Обзор популярных органических растворителей
Растворители органического происхождения получили активное распространение на территории постсоветского пространства за счет высокой устойчивости к суровым климатическим условиям.
Группа углеводородов
Бензин «Галоша», Нефрас
- Данные вещества получают в ходе перегонки малосернистой нефти. Они представляют собой прозрачную жидкость (допускается желтоватый оттенок) со сладковатым запахом. Главным отличием представленных продуктов является ярко выраженные свойства по растворению красок и эмалей.
- Их используется для разбавления ЛКМ, подготовки и очистки поверхностей. Эти сильные растворители востребованы в ювелирном деле, где требуется высокий результат при минимальных дозировках.
Скипидар
- Бесцветная и легковоспламеняющаяся жидкость - результат перегонки сосновой древесины или разгонки смолы хвойных пород (живичный скипидар). Температура ее воспламенения составляет 34 градуса.
- Резко пахнущий растворитель применяют для разжижения масляных и алкидных красок, лаков, а также для очистки инструментов. Он прекрасно подходит для обезжиривания поверхностей перед их покраской или склеивания.

Уайт-спирит
- Жидкое прозрачное вещество с острым специфическим запахом получается в результате смешивания алифатических и ароматических углеводородов. Субстанция характеризуется большой эффективностью по обезжириванию поверхностей и удалению масляных загрязнений.
- Кроме этого, он используется в качестве разбавителя алкидных эмалей, лаков, мастик на основе битума или каучука. Композит растворит жиры, нефтяные фракции, органические соединения кислорода, азота и др.
Ксилол
- Этот ароматический углеводород представляет собой бесцветную жидкость без посторонних примесей. Приятный запах не должен ввести в заблуждение, большая концентрация паров однозначно нанесет вред здоровью.
- Он легко справляется с такими функциональными задачами, как: растворение красок на основе эпоксидных смол, полимерных лаков, полиуретановых мастик. Низкая степень испарения обеспечивает более гладкую и блестящую поверхность.
Группа кетонов
Ацетон
- Бесцветная летучая жидкость с резким запахом легко воспламеняется. Ее получают в процессе синтеза фенола. Выгодно отличается хорошим смешиванием и с водой, и другими подобными растворителями.
- Он широко применяется для растворения нитроэмалей и нитролаков, а также некоторых солей: иодида калия, хлорида кальция. Способен расщепить жиры на резиновых поверхностях, удалить жирные и восковые загрязнения.

Метилизобутилкетон
- Данный растворитель не имеет цвета, обладает резким сладковатым запахом. Он является результатом конденсации ацетона с дальнейшей дегидратацией и гидрированием окиси мезитила.
- Его активно используют в качестве важного компонента при производстве красок на основе эпоксидных смол. Он прекрасно растворяет канифоль, каучук, сополимер винилхлорида, многие природные и синтетические смолы.
Циклогексанон
- Чуть вязкая бесцветная жидкость имеет очень резкий запах с мятным оттенком. Легко воспламеняющееся вещество схоже по свойствам с ацетоном. Его получают путем окисления циклогексана в присутствии нафтената.
- Незаменим при растворении нитратов, природных смол, масел, ацетатов целлюлозы, поливинилхлоридов. Вместе с этилацетатом подходит для разбавления большинства видов красок. Он является составной частью пятновыводителей.
Группа простых и сложных эфиров
Диоксан 1,4
- Это простой эфир, получаемый синтетическим путем. Он представляет собой бесцветную жидкость с сильным запахом. Легко растворяется в воде, спирте и смешивается с эфирами.
- Особо востребован при производстве нитро и ацетилцеллюлозных лаков. Применяется как растворитель для красок. Свободно расщепляет жиры, масла, воски и др. Подходит в качестве стабилизатора для хлорсодержащих растворителей.
Этилацетат
- Сложный эфир, не имеющий цвета, обладает приятным запахом (при небольших концентрациях). Получение осуществляется в результате переработки синтетической уксусной кислоты. Горючая жидкость характеризуется высокой растворимой способностью и летучестью.
- Его используют для очищения и обезжиривания поверхностей, а также растворения пленок, эфиров целлюлозы, пигментов, масляных красок, полиэфирных лаков, эмалей, смазочных масел.
Метилацетат
- Бесцветный этиловый эфир уксусной кислоты используется для растворения эфиров целлюлозы, большинства видов смол, жиров, лакокрасочной продукции. Может выступать в соединении с другими растворителями.
- По своим растворяющим способностям схож с ацетоном и вполне может использоваться как его заменитель. Однако метилацетат отличается высокой токсичностью, несмотря на приятный запах.
Группа спиртов
Этанол
- Легкоподвижную жидкость с характерным запахом получают путем анаэробного брожения углеводородов растительного происхождения. Легко воспламеняется при контакте с огнем.
- Технический спирт применяют при производстве лакокрасочной продукции. Широко используются для дезинфекции, а также обезжиривания поверхностей перед дальнейшим их окрашиванием или склеиванием.

Метанол
- Бесцветный одноатомный спирт отличается повышенной воспламеняемостью и характерным запахом. Его получение производится синтетическим способом. Легко смешивается с водой и большинством органических растворителей (этанолом, ацетоном, бензолом).
- Он нашел широкое применение при изготовлении ЛКМ. Из-за высокой токсичности запрещено использование метанола в ряде потребительских товарах.
Бутанол
- Слегка вязкая жидкость не имеет цвета, но обладает характерным сивушным запахом. Ее получение основывается на процессе оксосинтеза из ацетальдегида. Является важным компонентом при производстве ЛКМ, пластификаторов и смол.
- Химические свойства органических растворителей позволяют растворять олифы, лаки, краски, каучуки, природные и синтетические смолы. Применим для удаления наслоений и загрязнений различного происхождения.
Правила работы с органическими растворителями
Большая часть растворителей органического происхождения негативно влияют на здоровье человека. Тяжесть воздействия определяется их видом. Чтобы исключить отравление или хотя бы снизить токсичное действие необходимо при работе с ними соблюдать правила безопасности.
- Использование индивидуальных средств защиты, то есть не пренебрегать очками, перчатками, респираторными масками.

- При попадании на кожу вещество немедленно вытереть сухой чистой тканью и промыть под проточной водой.
- Помещение, выделенное под работы, должно быть оснащено вентиляционной системой. В крайнем случае, открываются окна, входные двери.
- Важно следить за температурой в рабочем боксе, некоторые растворители взрывоопасны. В связи с этим запрещается их использование в непосредственной близости от горячих (раскаленных) предметов.
- Тара с органическими растворителями транспортируется и хранится в прохладных помещениях строго в вертикальном положении (горлышком вверх).
Безопасность и здоровье
Способность растворяться в жирах и летучесть органических растворителей обуславливает их токсичное воздействие на здоровье человека. Обычно негативное воздействие происходит через дыхательные пути и кожу.
- Отравление проявляется в следующих симптомах: раздражение кожных покровов, слизистой оболочки дыхательных органов, пищеварительной системы. При острой токсичности может появиться шум в ушах, тошнота, возбуждение, онемение подушечек пальцев, потливость, аритмичное сердцебиение.
- В производственных условиях, где, как правило, происходит длительной контакт с веществами небольшой концентрации, у работников развивается хроническое отравление. Оно сопровождается плохим аппетитом, усталостью, сонливостью, потерей веса.
Специфическое действие органических растворителей может проявиться в любых признаках, а также их сочетаниях.
- Углеводороды ароматического ряда вызывают раздражение центрально-нервной системы, изменение картины крови. На коже может появиться покраснение, сопровождающееся зудом.
Для рабочих помещений концентрация в воздухе паров бензола должна составлять не более 5 мг/м.куб., для толуола и ксилола - 50 мг/м.куб.
- Углеводороды жирного ряда . Сюда входят такие популярные растворители, как бензин, петролейный эфир и уайт-спирит. При хроническом отравлении наблюдается психическая нестабильность, дрожание век и вытянутых рук. Наличие хлора в углеводородах жирного ряда (хлорзамещенные вещества) придает специфическое воздействие на внутренние органы, развивает анемию, расстраивает сердечную деятельность.

Для рабочих помещений концентрация в воздухе паров для смеси алифатических и ароматических углеводородов должна составлять не более 100 мг/м.куб., для четыреххлористого углерода - до 2 мг/м.куб., дихлорэтана - 10 мг/м. куб.
- Спирты поступают в организм через дыхательные пути или кожу. Углеродные атомы медленно накапливаются в организме и еще медленнее выводятся. Среди распространенных признаков отравления можно отметить: головные боли, атрофию зрительного нерва, а также хронические заболевания почек, сердца.
Для рабочих помещений концентрация в воздухе метанола не должна превышать 5 мг/м.куб., для пропилового и бутилового спирта - 10 мг/м.куб.
- Сложные эфиры оказывают сильное воздействие на здоровье человека. При длительном вдыхании появляется головная боль, повышенное сердцебиение, снижение зрения, раздражение слизистых оболочек глаз.
Для рабочих помещений концентрация в воздухе паров сложных эфиров должна составлять не более 100 мг/м.куб.
- Кетоны. Популярным растворителем данной группы выступает ацетон. Его большая концентрация приводит к острому отравлению, симптомами которого является анемия, раздражение слизистых оболочек, головокружение, слезотечение.

Для рабочих помещений концентрация в воздухе паров кетонов должна составлять не более 200 мг/м.куб.
- Сероуглерод это высокотоксичное вещество. При тяжелых отравлениях замечено нарушение психики, расстройство желудочно-кишечного тракта, ослабление памяти, дрожание рук, потеря зрения.
Для рабочих помещений концентрация в воздухе паров сероуглерода должна составлять до 1 мг/м.куб.
- Нитро- и аминопроизводные и их гомологи представляют расширенную группу растворителей. Хроническая картина отравления выражается в виде головной боли, апатии, синюшного цвета кожи, нарушения работы печени и центральной нервной системы.
Для рабочих помещений концентрация в воздухе паров аналина должна составлять не более 0,1 мг/м.куб, соединения бензола и толуола - до 1 мг/м.куб.
Уничтожение отходов
- Проблема с утилизацией актуальна в промышленной деятельности. Некоторые предприятия обращаются за помощью в специализированные компании. Уничтожение должно быть безотходным и безвредным как для человека, так и окружающей среды.
- Химические соединения и их смеси токсичны, активны, а многие из них пожаро- и взрывоопасны. Испарения, производимые этими летучими веществами, наносят непоправимый вред людям и природе. Поэтому к процессу необходимо подходить с соблюдением правил безопасности, включая использование средств личной защиты.
Cтраница 1
Углеводородные растворители - пироконденсат, КОН-47-88 и отработанный керосин не содержат парафина, смол и других природных эмульгаторов, поэтому они не образуют с водой или же с ингибировэнной соляной кислотой эмульсий. Эмульсия, приготовленная с перечисленными растворителями и раствором кислоты или воды, расслаивается через несколько минут после приготовления. Если в растворе содержится 0 5 % и более эмульгатора СКН-26, данная смесь при температуре 30 С не течет.
Углеводородные растворители нашли широкое применение в лакокрасочной промышленности благо-даря их низкой стоимости и доступности, К этой группе растворителей относятся предельные углеводороды алифатического ряда (парафины, или алка-ны) СлН2я 2, алициклические углеводороды общего состава С Н2 и ароматические углеводороды.
Углеводородный растворитель - кубовый остаток нефти - КОН - 47 - 88 является производственным отходом отечественных заводов химической промышленности. Плотность смеси 850 - 900 кг / м3, кинематическая вязкость при 20 С 2 1 мПа - с, температура начала и конца кипения 88 - 180 С.
Углеводородный растворитель при этом практически не влияет на ползучесть монокристаллов олова, являясь, таким образом, неактивной средой.
Углеводородные растворители широко применяются в самых различных отраслях промышленности. Их применение определяется удачным сочетанием высокой растворяющей способности углеводородов по отношению к широкому кругу органических соединений с относительно малой токсичностью и отсутствием коррозионной активности.
Углеводородные растворители характеризуются средней молекулярной массой.
Углеводородные растворители по сравнению с рассмотренными являются более мягкими; оин не удаляют красители с текстильных материалов и не вымывают природный жир из волокон шерсти, замшн н кожи. Однако они растворяют жиры, пчелиный воск, рыбий жир, потосальные выделения, растительные и смазочные масла, деготь, ваксу, парафин, пек, канифоль, каучук, битум н другие вещества. Эти растворители не разрушают такие волокна, как ацегохлорнн, поливинилхлоридные, поливинилидеихло-ридные и др. Они менее токсичны и достаточно дешевы. Недостатком углеводородных растворителей является горючесть н взрывоопасность их смесей с воздухом.
Углеводородные растворители относятся к пожаровзрывоопасным токсичным веществам. Большинство из них характеризуется высокой испаряемостью. Пары растворителей в несколько раз тяжелее воздуха, они скапливаются в низких местах в плохо вентилируемых помещениях и около аппаратов, что может привести к взрыву или отравлению.
// Растворители
Растворителями называются химические соединения, которые способны растворять различные вещества, т.е. образовывать с ними однородные смеси переменного состава из двух или более компонентов.
Растворитель является одним из самых необходимых компонентов при производстве пленкообразующих веществ. Самый распространенный растворитель в природе - это обычная вода, но в лакокрасочной промышленности этот растворитель используется, в основном, в производстве воднодисперсионных красок, грунтовок и лаков. Среди растворителей для красок, эмалей и лаков гораздо более широкое распространение получили органические растворители. Все используемые лакокрасочной промышленностью органические растворители по химической природе можно разделить на следующие шесть групп:
1) углеводороы - алифатические, алициклические, ароматические, а так же нефтяные и терпеновые;
2) кетоны;
3) простые и сложные эфиры;
4) спирты;
5) галогенсодержащие растворители;
6) прочие растворители.
Углеводородные растворители нашли широкое применение в лакокрасочной промышленности из-за их низкой стоимости и широкой доступности.
К этой группе растворителей относятся предельные углеводороды алифатического ряда (парафины или алканы), алициклические углеводороды и ароматические углеводороды.
Углеводородные растворители получают при сухой перегонке дерева и каменного угля, из сланцевого бензина, из нефти и нефтяного газа.
В настоящее время основным природным источником большинства углеводородных растворителей является нефть.
В ней, в основном, содержатся парафиновые, нафтеновые и ароматические углеводороды. В зависимости от типа нефти в ней преобладает тот или иной класс углеводородов.
А вот фракции нефти, перегнанные в широком диапазоне температур, состоят из смеси углеводородов различного химического строения.
Алифатические углеводороды - в лакокрасочной промышленности находят применение преимущественно парафины.
За рубежом широкое применение нашли изопарафины, так как они практически не имеют запаха (запах органических растворителей обусловлен их высокой летучестью и относится к вредным факторам работы с растворителями). Изопарафины применяются для создания малотоксичных покрытий, в медицине при производстве хирургических шовных материалов и т. п.
Алициклические углеводороды имеют ограниченное применение в производстве и технологии нанесения лакокрасочных покрытий, хотя и обладают более высокой растворяющей способностью, чем алифатические растворители, и меньшей токсичностью по сравнению с ароматическими. Основным природным источником получения этих растворителей является нефть.
Алициклические растворители достаточно широко используются в производстве синтетических волокон, резни, печатных красок.
Наибольшее применение в качестве растворителя получил циклогексан, который применяется для растворения этилцеллюлозы, масел и жиров, восков и каучуков.
Ароматические углеводороды - наиболее обширная группа углеводородных растворителей, выпускаемых химической промышленностью.
В настоящее время ароматические углеводороды получают преимущественно из нефтяных фракций методами каталитического риформинга и пиролиза и, значительно в меньшей степени, при переработке каменного угля.
Отечественной промышленностью выпускаются практически все ароматические растворители.
Ароматические растворители обладают более высокой растворяющей способностью по сравнению с другими углеводородными растворителями и в качестве составляющих компонентов входят в большинство смесевых растворителей.
К ароматическим растворителям относятся: бензол, толуол и ксилол, изопропилбензол, сольвент, тетралин и декалин.
Для характеристики нефтяных растворителей, объединяемых термином "нефрас" (нефтяной растворитель), используются признаки, характеризующие их углеводородный и фракционный составы; последние же определяют основные физико-химические свойства растворителей.
Указываются также и другие параметры, такие,например,как температура вспышки.
Различают следующие типы нефтяных растворителей по их углеводородному составу:
Нефрас-С - растворители смешанного состава, в которых присутствуют углеводороды всех групп (но не более 50% массовой доли углеводородов каждой из групп).
Нефрас-А - растворители с преобладанием алифатических углеводородов и пониженным содержанием ароматических углеводородов (не более 2,5%).
Нефрас-И - изопарафиновые растворители.
Нефрас-П - парафиновые, содержащие более 50% массовой доли парафиновых углеводородов.
Нефрас-Н - с преобладанием нафтеновых углеводородов.
Важнейшими эксплуатационными свойствами нефтяных растворителей являются:
Способность растворять органические соединения;
Способность удалять органические загрязнения с поверхности металлов;
Способность быстро испаряться;
Способность к минимальному образованию отложений своих компонентов;
Коррозионная агрессивность (определяется наличием в растворителях сернистых соединений);
Стабильность качества нефтяных растворителей, которая характеризуется их гарантийным сроком хранения.
Примерами нефтяных растворителей являются: бензины, уайт-спирит, гексановые и гептановые растворители.
Терпеновые углеводороды являются одним из давно известных классов растворителей растительного происхождения.
К ним относятся природные и синтетические углеводороды.
Терпены содержатся в эфирных маслах цветов, листьях различных растений, в природных смолах (бальзамах), в хвое и древесине хвойных деревьев (сосны, ели, пихты, можжевельника, лиственницы).
К числу широко применяемых терпеновых растворителей относятся скипидар, дипентен, сосновое масло (пайнойль), изопропилтолуол.
Кетоны являются растворителями большинства пленкообразующих веществ.
В лакокрасочной промышленности применяются алифатические и циклические кетоны.
Из алифатических предельных кетонов широко используются: ацетон, метилэтилкетон, метилизобутилкетон, диизобутилкетон, диацетоновый спирт.
Основным достоинством алифатических кетонов является их высокая растворяющая способность и сравнительно малая токсичность.
Из циклических кетонов нашли применение циклогексанон и метилциклогексанон.
Они обладают более высокой токсичностью, чем алифатические кетоны.
К простым эфирам относятся производные одноатомных и двухатомных (гликолей) спиртов и их циклические соединения.
Из производных одноатомных алифатических спиртов находят применение диэтиловый и дибутиловый эфиры.
Наибольший интерес представляют моноалкиловые эфиры этиленгликоля - целлозольвы и диэтиленгликоля - карбитолы.
Сложные эфиры - самый распространенный класс органических растворителей, имеющих огромное практическое применение.
Сложные эфиры получают этерификацией соответствующих спиртов минеральными или органическими кислотами.
Н аибольшее применение в качестве растворителей получили эфиры уксусной кислоты - ацетаты(метилацетат, этилацетат, бутилацетат).
Прочие эфиры (кислот молочной - лактаты, масляной - бутираты, муравьиной - формиаты) нашли ограниченное применение, в том числе и из-за их достаточно высокой стоимости.
Формиаты из-за сильной омыляемости и высокой токсичности в настоящее время почти не используются.
Спирты тоже получили широчайшее применение в качестве растворителей.
Наиболее распространены метанол, этиленгликоль, глицерин, пентаэритрит, бутанол, изопропанол.
Среди растворителей широкое распространение имеют самые разные классы спиртов: одноатомные и многоатомные; алифатические и циклические.
Спирты относятся к полярным растворителям и применяются в самых различных отраслях промышленности.
Самым распространённым спиртом среди растворителей является этанол - его мировой объём потребления в этом качестве немного не достигает 4 млн тонн в год.
Другими популярными растворителями являются метанол и изопропанол с объёмами потребления в этом качестве более 1 млн тонн в год.
Использование спиртов в качестве растворителей включает в себя следующие направления: технологический растворитель, растворитель в производстве красок и покрытий, очиститель, растворитель в производстве потребительской продукции, аэрозольный растворитель.
Галогеносодержащие растворители (хлорметаны, хлорэтаны, фторхлорсодержащие растворители, водородные фторалканы) обладают наибольшей растворяющей способностью, и на их основе получают качественные средства для обезжиривания.
Такие растворители используются, в частности, для обезжиривания кислородных баллонов или манометров.
Данные растворители отличаются пониженной горючестью, они обладают лучшей испаряемостью, чем большинство растворителей, и более эффективные.
Их основным недостатком является очень высокая токсичность.
Их применение вносят немалый "вклад" в парниковый эффект и "кислотные" дожди, и по этой причине их относят к материалам, приводящим к разрушению озонового слоя атмосферы Земли. Из-за этого, понятно, они пользуются очень большой нелюбовью экологов.
Растворители должны обладать химической инертностью по отношению к растворяемому веществу, т.е. не должны вступать в химическое взаимодействие с ним.
Растворители должны обладать низкой гигроскопичностью: даже при незначительном количестве воды их растворяющая способность резко снижается.
Органические растворители токсичны, они (и их пары) оказывают вредное воздействие на человека.
При работе с ними необходимо строго соблюдать меры безопасности, в частности обеспечивать хорошее проветривание помещений, а в необходимых случаях применять защитные средства - перчатки и респираторы.
При работе с растворителями необходимо учитывать их пожароопасность.
Подавляющее большинство органических растворителей горючи, а смесь их паров с воздухом при определенной концентрации образует взрывоопасную смесь.
Поэтому в помещениях, где хранятся растворители и ведутся работы с ними, надо строго соблюдать правила противопожарной безопасности.
