Węglowodory alifatyczne. Rodzaje rozpuszczalników.
Substancje takie jak rozpuszczalniki są regularnie stosowane zarówno w życiu codziennym, jak iw przemyśle. Na pewno będą potrzebne w tym procesie. prace remontowe w domu i nie ma nic do powiedzenia o dużych przedsiębiorstwach przemysłowych, niektóre procesy po prostu nie są możliwe bez użycia rozpuszczalników.
Co to jest rozpuszczalnik i jaki jest jego cel
Rozpuszczalnik to szybko odparowująca płynna substancja chemiczna lub mieszanina kilku substancji organicznych, która ma zdolność rozpuszczania lepkich substancji organicznych w celu utworzenia jednorodnej mieszaniny.
Zasadniczo rozpuszczalnik jest przeznaczony do powłok malarskich i lakierniczych, a mianowicie doprowadzenia ich do wymaganej konsystencji przed użyciem. Niektóre barwniki nie mogą być stosowane bez rozpuszczalnika, na przykład te o wysokim stężeniu i przechowywane w specjalnym pojemniku.

Rozpuszczalnik wysokiej jakości, w zależności od swojego przeznaczenia, musi spełniać następujące wymagania:
- łatwo miesza się z farbą do uzyskania gładkości;
- po nałożeniu barwnika lub lakieru rozpuszczalnik powinien szybko wyparować;
- mieszając z koncentratem barwnika, rozpuszczalnik nie powinien zacząć z nimi reagować;
- właściwości rozpuszczalnika nie powinny się zmieniać w kontakcie z wodą.
Krótko mówiąc, przeznaczenie rozpuszczalnika można scharakteryzować następująco: zapewnienie wygody nakładania barwnika na powierzchnię, a następnie szybkie i niepostrzeżenie znikanie. Stosuje się je również przed rozpoczęciem prac malarskich, odtłuszczaniem powierzchni roboczych, a także po ich zakończeniu, czyszczeniu narzędzia.
Każda pozycja z linii farb i lakierów wymaga użycia określonego rodzaju rozpuszczalnika. Konieczne jest obserwowanie zgodności rozpuszczalnika z rodzajem farby, aby uzyskać jednorodną substancję, która nie rozpadnie się na części składowe i umożliwi jej rozprowadzenie na wymaganym obszarze.
Rodzaje rozpuszczalników
Rozpuszczalniki dzielą się na dwa typy:
- organiczny;
- nieorganiczny.

Rozpuszczalniki organiczne są najbardziej popularne w porównaniu z nieorganicznymi, a zgodnie z ich właściwościami fizycznymi istnieją następujące typy:
- trudne do ulatniania się, takie jak terpentyna. Mają zastosowanie do emalii i lakierów;
- średnio lotne, takie jak nafta. Najczęściej stosuje się je do farb olejnych i akrylowych;
- lotne, takie jak benzyna, benzyna lakowa, rozpuszczalnik. Stosowane są do emalii, lakierów, barwników akrylowych i olejnych. Podczas interakcji z tą grupą rozpuszczalników należy zachować szczególną ostrożność i być ostrożnym, ponieważ wysoce lotne substancje są niezwykle wybuchowe.
Najczęściej są to mobilne substancje płynne, o charakterystycznym silnym zapachu, co jest jedną z głównych wad.
Lista nie jest rozpuszczalniki organiczne obejmuje:
- woda;
- ciekły amoniak;
- sole siarkowe, fosforowe i inne.

Rozpuszczalniki organiczne, w przeciwieństwie do nieorganicznych, mają szereg poważnych wad, w tym utrzymujący się przez dłuższy czas zapach oraz łatwopalne toksyczne opary, które mogą również prowadzić do poważnych zatruć.
Niestety, barwniki rozpuszczalne w wodzie, które są bardziej poszukiwane za granicą, nie są jeszcze bardzo poszukiwane w naszym kraju ze względu na utratę jakości podczas przechowywania w surowym rosyjskim klimacie.
Przegląd najczęściej stosowanych w naszym kraju rozpuszczalników, ich właściwości
Rozpuszczalniki organiczne, mimo że wcale nie są bezpieczne, są szeroko stosowane w Rosji, czego nie można powiedzieć o ich nieorganicznych odpowiednikach. Rozpuszczalniki dzielą się na trzy grupy:
- węglowodór;
- alkohol;
- estry.
Poniżej rozważymy cechy i właściwości najczęstszych. Rozpuszczalniki węglowodorowe obejmują:
- Benzyna lakowa jest bezbarwną, oleistą cieczą. Jest wyjątkowo łatwopalny i ma zapach podobny do nafty. Jego wydajność rozpuszczania nie jest bardzo wysoka, ale mimo wszystko benzyna lakowa jest nadal poszukiwana ze względu na względną taniość i nietoksyczność.
- Benzyna z ropy naftowej. Bezbarwna ciecz, która szybko odparowuje i nie jest rozpuszczalna w wodzie. Posiada silny zapach jak również wszystkie substancje z grupy organicznej. Benzen naftowy jest kompatybilny ze związkami węglowodorowymi. Wydziela toksyczne, palne opary, w kontakcie z powietrzem staje się wybuchowy.
- Terpentyna. Jest podzielony na gumę i pneumatykę. Guma jest najlepsza. Jest to bladożółta ciecz o ostrym zapachu, używana do rozcieńczania szpachli i oleistych farb.
- Benzyna. Produkt rafinacji ropy naftowej ma właściwości palne i łatwo odparowuje. Po osiągnięciu pewnej ilości oparów w powietrzu może wybuchnąć.

Rozpuszczalniki alkoholowe obejmują:
- Etanol. Jest płynny, nie ma koloru, ale ma rozpoznawalny zapach. Nie powinien zawierać różnych obcych cząstek. Jego opary mogą powodować poważne zatrucia, pod warunkiem, że duża ich ilość dostanie się do dróg oddechowych. Nie tylko łatwo się zapala w kontakcie z ogniem lub iskrami, ale może zapalić się po prostu pod wpływem wysokich temperatur.
- Alkohol butylowy. Stosowany jako rozcieńczalnik do lakierów nitrocelulozowych. Powłoka nabiera połysku, staje się gładsza, a także staje się mniej podatna na wybielanie.
- Alkohol metylowy (metanol). Przejrzysta, płynna substancja, zwykle zawierająca domieszkę eterów i acetonu. Jest niezwykle trujący.
- Glikol etylenowy. Przezroczysta, bezwonna, lepka ciecz. Tworzy jednorodne wiązanie z wodą. Długo paruje, przez co jest niezastąpiony przy pracy z lakierami nitro, których powłoka jest błyszcząca, gładka, łatwa do polerowania.
Estry są reprezentowane przez następującą grupę rozpuszczalników:
- Octan metylu. Szybko odparowująca, płynna, ruchliwa substancja o właściwościach toksycznych i pożarowych. Wrze w temperaturze 56-58 stopni.
- Octan etylu. Odparowuje nie tak szybko, wrze w temperaturze 77-82 stopni, ma przyjemny zapach.
- Octan butylu. Płynny, ma żółtawy odcień, długo odparowuje i dlatego jest stosowany w przypadku konieczności wydłużenia czasu schnięcia powłoki.
- Octan amylu. Przejrzysty, płynny, ma przyjemny zapach, powoli odparowuje. Podobnie jak octan butylu służy do opóźniania suszenia.
- Aceton. Ma charakterystyczny i bardzo nieprzyjemny zapach, jest niezwykle lotny i niebezpieczny dla ognia.
- Mieszaniny rozpuszczalników. Do rozcieńczenia stężonych lakierów nitro do pożądanej lepkości stosuje się mieszaniny rozpuszczalników z grupy estrowej. Jednocześnie właściwości jakościowe powłoki zależą bezpośrednio od elementów kompozycji. Na przykład, jeśli zawiera największa liczba szybko odparowujących rozpuszczalników powłoka może stać się mętna, ale jeśli zrobisz mieszaninę substancji, które spowalniają czas schnięcia, powłoka będzie błyszcząca, gładka i przejrzysta.
Przegląd numerowanych rozpuszczalników
Istnieje tak ogromna różnorodność rozpuszczalników, że aby je odróżnić, niektórym z nich zaczęto przypisywać numery, które umożliwiają poruszanie się po nazwach i dokonywanie wyboru. Rozważmy najczęstsze:
- Rozpuszczalnik 4 (R-4) jest szeroko stosowany. W rzeczywistości jest to mieszanina zawierająca aceton i toluen. Zasadniczo P-4 stosuje się do lakierów i farb alkidowych, a także emalii na bazie chlorowanych polimerów. Składniki obecne w rozpuszczalniku dobiera się tak, aby zapewnić pozytywny wpływ na konsystencję i tworzenie powłoki substancji błonotwórczych.
W razie potrzeby można go również użyć do odtłuszczenia powierzchni przed powlekaniem, ale jeśli to możliwe, lepiej jest wziąć do tego inny rozpuszczalnik. P-4 jest niezwykle lotny.

Jest łatwopalny i należy się z nim obchodzić ostrożnie i przy użyciu środków ochrony osobistej.
- Jeszcze bardziej popularny jest rozpuszczalnik 646, niezbędny zarówno w życiu codziennym, jak iw przemyśle. Nadaje się zarówno do rozpuszczania, jak i odtłuszczania i jest używany w różnych zastosowaniach, w tym w warsztatach samochodowych. Thinner 646 ma doskonałe właściwości jakościowe. Zawiera całą listę takich składników, dzięki czemu staje się wielofunkcyjny, może rozpuszczać wiele różnych związków chemicznych.
Rozcieńczalnik 646 ma żółtawy odcień i ostry zapach, szybko odparowuje. Zawiera węglowodory aromatyczne, ketony, alkohole, etery. W trakcie korzystania z niego musisz być bardzo ostrożny, ponieważ z powodu jego świetna aktywnośćłatwo zepsuć poprzednie warstwy barwnika. Czasami, ze względu na tę właściwość, rozpuszczalnik 646 jest nawet zastępowany słabszymi.
Bez tego niemożliwe jest wytwarzanie i stosowanie wielu rodzajów farb i lakierów. Rozpuszczalnik 646 jest albo używany podczas wytwarzania tego produktu, albo rozcieńczany do pożądanej konsystencji przed użyciem. Jest również niezbędny do rozcieńczania niektórych wypełniaczy.
Rozcieńczona rozpuszczalnikiem 646 farba po wyschnięciu staje się błyszcząca i gładka. Powłoki emalii i lakierów, w których została zastosowana, po nałożeniu szybko i łatwo wiążą, tworząc film. Gdy rozpuszczalnik 646 wyparuje, zapach znika.
Kolejną zaletą, dzięki której konsumenci pokochali ten rozpuszczalnik, jest cena, która pomimo wszystkich swoich pozytywnych cech jest dość niska, a także jego dostępność w domenie publicznej - w każdym supermarkecie budowlanym można kupić 646 rozpuszczalników.
- Rozpuszczalnik 2 (PC-2) również ma dobre właściwości. Jest to klarowny płyn o jasnożółtym odcieniu. Szybko odparowuje. Zawiera ksylen i benzynę lakową. Są rozcieńczane lakierami olejnymi, farbami bitumicznymi, emaliami pentaftalowymi. Wydziela niezwykle toksyczne opary. Podczas pracy z PC-2 należy zawsze chronić skórę i drogi oddechowe oraz oczy. Pary mają również szkodliwy wpływ na układ nerwowy, narządy wewnętrzne, krew i szpik kostny, dostając się do organizmu nie tylko przez drogi oddechowe, ale także przez skórę.
Oprócz wpływu wewnętrznego substancja może mieć również wpływ zewnętrzny, na przykład wywołać wysypkę przy długotrwałym kontakcie.
Substancja jest łatwopalna, w przypadku nagromadzenia oparów w powietrzu może dojść do wybuchu.
Obszary zastosowania rozpuszczalników
Jak wspomniano powyżej, rozcieńczalnik do farby jest wymagany do następujących prac:
- rozcieńczanie zagęszczonej lub silnie skoncentrowanej emalii oraz farb i lakierów;
- czyszczenie przedmiotów lub odzieży poplamioną farbą;
- czyszczenie narzędzi używanych do malowania i lakierowania.
Rozpuszczalniki są używane w wielu dziedzinach. Ma swój własny dla każdego typu. Na przykład aceton jest z powodzeniem stosowany w syntezie poliwęglanów, żywic epoksydowych i poliuretanów. Rozpuszcza w nim oleje, żywice naturalne, poliakrylany, chlorokauczuk, a także tłuszcze, woski, gumę.
Benzyna lakowa ma zastosowanie do wszelkich farb i lakierów. Nadaje się do farb olejnych, lakierów, emalii, podkładów, mas samochodowych. Odtłuszczają powierzchnie, czyszczą narzędzie.

Nafta, benzyna i inne węglowodory służą do rozpuszczania tłuszczów, olejów, parafiny, wosków.
Rozpuszczalniki należące do grupy eterowej, np. octan etylu, octan butylu, rozpuszczają polarne żywice syntetyczne, cerryzynę.
Rozpuszczalniki z grupy alkoholi, etylowy, butylowy, metylowy i inne wykorzystywane są do produkcji lakierów, a także do rozpuszczania żywic poliestrowych i nitrocelulozy.
Zasady pracy z rozpuszczalnikami
Prawie wszystkie rozpuszczalniki organiczne mają pewien stopień dotkliwości dla zdrowia ludzkiego, w zależności od gatunku. Aby nie cierpieć z powodu toksycznych oparów podczas pracy z nimi, należy ściśle przestrzegać środków ostrożności:
- podczas pracy używać środków ochrony osobistej, takich jak rękawice, respirator, okulary itp .;
- jeśli substancja dostanie się na skórę, należy ją zmyć natychmiast, zanim będzie miała czas na działanie lub ma minimalny wpływ;
- zapewnić dostęp do pomieszczenia z wystarczającą ilością świeżego powietrza;

- konieczne jest kontrolowanie temperatury w pomieszczeniu, ponieważ niektóre rozpuszczalniki stają się wybuchowe w kontakcie z ciepłym powietrzem;
- należy również wziąć pod uwagę palność i palność tych substancji, niedopuszczalne jest wykonywanie pracy w pobliżu otwartego ognia, palenie jest również niebezpieczne lub po prostu obecność gorących przedmiotów w pobliżu;
- musisz przechowywać rozpuszczalniki w chłodnym pomieszczeniu, w małych butelkach lub puszkach, które muszą mieć na nich etykiety;
- wszystkie pojemniki muszą być zakorkowane, niedopuszczalne jest leżenie na boku lub zakorkowanie.
Artykuł poświęcony jest różnym aspektom wykorzystania rozpuszczalników w procesach technologicznych wytwarzania sprzętu elektronicznego i nie tylko.
Informacje ogólne
Rozpuszczalniki to pojedyncze związki chemiczne lub ich mieszaniny zdolne do translacji różne substancje do rozwiązania. Z kolei rozwiązania są jednorodne systemy jednorodne składający się z dwóch lub więcej składników, których skład, w pewnych granicach, może być stale zmieniany. Dominujący składnik nazywa się rozpuszczalnikiem, reszta to substancje rozpuszczone. Rozróżnij roztwory gazowe, ciekłe i stałe. Gaz obejmuje powietrze, palne gazy naturalne itp. W praktyce często mamy do czynienia z roztworami płynnymi.
Zazwyczaj jako medium do prowadzenia reakcji chemicznych lub do celów technologicznych stosuje się rozpuszczalniki. Powstawanie roztworów znacząco zmienia warunki zachodzenia reakcji chemicznych między składnikami. Co więcej, wiele procesów może odbywać się tylko w rozwiązaniach. Rozpuszczalniki tworzą jednorodne środowisko, zapewniając kontakt między reagującymi cząstkami (jonami, cząsteczkami), a także wpływają na mechanizm reakcji chemicznych, ich szybkość, ustalenie równowagi itp. W reakcjach egzotermicznych rozpuszczalniki rozcieńczające reagenty pomagają usunąć nadmiar ciepło. Rozpuszczalniki jako narzędzie technologiczne znajdują szerokie zastosowanie w różnych dziedzinach techniki (w produkcji lakierów i farb, materiałów wybuchowych, w farmacji, perfumerii, rolnictwie itp.). Rozpuszczalniki są szeroko stosowane w większości mikro i makrotechnologii stosowanych w produkcji sprzętu elektronicznego.
Jak wszystkie związki chemiczne, rozpuszczalniki dzielą się na nieorganiczne i organiczne. Najważniejszym rozpuszczalnikiem nieorganicznym jest woda. Mniej znane rozpuszczalniki nieorganiczne to niskotopliwe halogenki (na przykład BrF3), oksohalogenki (na przykład chlorek sulfurylu, chlorek tionylu), rozpuszczalniki zawierające azot (ciekły amoniak) itp. Zakres rozpuszczalników organicznych jest znacznie szerszy.
Rozpuszczalniki można sklasyfikować według ich właściwości fizyczne.
Rozpuszczalniki o temperaturze wrzenia poniżej 100 ° C klasyfikowane są jako rozpuszczalniki niskowrzące, o temperaturze wrzenia powyżej 150 ° C - jako rozpuszczalniki wysokowrzące.
W zależności od stopnia lotności rozpuszczalniki dzielą się na lotne, średniolotne i nielotne.
W zależności od lepkości rozpuszczalniki dzielą się na o niskiej lepkości (poniżej 2 mPa-s), średniej lepkości (2-10 mPa-s) i wysokiej lepkości (powyżej 10 mPa-s).
W zależności od obecności / braku momentu dipolowego i wartości stałej dielektrycznej rozróżnia się rozpuszczalniki polarne i niepolarne. Wyróżnia się cztery grupy rozpuszczalników w zależności od stałej dielektrycznej i właściwości donora-akceptora.
1. Rozpuszczalniki protonowe (woda, alkohole, kwasy karboksylowe itp.). Są donorami protonów i mają wysoką stałą dielektryczną (ε>15).
2. Aprotonowe rozpuszczalniki bipolarne (niektóre aprotonowe amidy, ketony, sulfotlenki). Mają wysoką stałą dielektryczną, ale nie mają właściwości dawcy-akceptora.
3. Rozpuszczalniki elektronodonorowe (etery).
4. Niepolarne rozpuszczalniki o niskiej stałej dielektrycznej (ε< 15). Это сероуглерод, углеводороды. Такие растворители не обладают донорно-акцепторными свойствами ни по отношению к протонам, ни по отношению к электронам.
W zależności od właściwości kwasowo-zasadowych rozpuszczalniki mogą być kwaśne (kwas octowy), zasadowe (pirydyna), obojętne (benzen).
Istnieje wiele opcji klasyfikacji rozpuszczalników, a także wszelkich związków chemicznych.
Cudowna cząsteczka
Bez zastanowienia możemy powiedzieć, że najpowszechniejszym rozpuszczalnikiem na Ziemi jest woda. Czasami nawet mówią, że bardziej słusznie byłoby nazywać naszą planetę Wodą. Powód jest prosty: woda zajmuje około 70% powierzchni ziemi. Ilość wody na Ziemi szacuje się na 1,39T0 18 ton. Naukowcy, aby udowodnić, że życie (życie organiczne) jest możliwe w tym czy innym zakątku Wszechświata, szukają tam śladów wody. I znajdują to! Cząsteczki wody znajdują się w przestrzeni międzygwiazdowej. Woda jest częścią komet, większości planet Układ Słoneczny... Co to jest, ta niesamowita, cudowna iw pewnym stopniu niezastąpiona cząsteczka?
Tak zwana formuła brutto wody (H 2 0) jest znana nawet podwójnie. Stereometrię, a raczej planimetrię tej cząsteczki podano poniżej.
L. Salem w swojej książce „Cudowna cząsteczka” posługuje się porównaniem cząsteczki wody z brzoskwinią, do której przyczepione są dwie morele. Brzoskwinia w środku to atom tlenu. Dwie małe morele po bokach to atomy wodoru. Atomy wodoru i tlenu znajdują się w rogach Trójkąt równoramienny... Aby oszacować wielkość cząsteczki wody, wystarczy podać długość komunikacja O-N... Jest równy 0,0957 nm.
Ponieważ atomy wodoru i tlenu mają różną elektroujemność, a wiązania chemiczne O-H znajdują się pod kątem innym niż 180 ° (104,5 °), cząsteczka wody jest polarna (dipol). Ponadto jest również polaryzowalny. Właściwości te w dużej mierze determinują zachowanie wody podczas interakcji z innymi związkami chemicznymi.
Woda ma bardzo wysoką stałą dielektryczną. W temperaturze pokojowej ε = 78,3. Całkowicie czysta woda jest dość dobrym izolatorem: właściwa rezystancja objętościowa izolacji wodnej w 0 ° C wynosi 1,47-10 b Ohm-m, w 50 ° C - 18,9 · 10 -6 Ohm-m. Można nawet powiedzieć, że jest to doskonały izolator, ale utrudnia to fakt, że niewielka część cząsteczek wody (około 1 na 5-10 -9) ulega dysocjacji elektrolitycznej według schematu:
![]()
Stężenie jonów H + (a właściwie H 3 0 +) i związane z tym stężenie jonów OH + charakteryzuje pH (pH pożywki). W praktyce na właściwości przewodnictwa wody znacznie większy wpływ mają rozpuszczone w niej sole, kwasy, zasady - stali towarzysze nie idealnie czystej, ale prawdziwej wody. Nawet niewielka koncentracja tych składników wystarczy, aby woda, jak za dotknięciem czarodziejskiej różdżki, zamieniła się z dielektryka w przewodnik.
Woda jest związkiem chemicznym, nie wspominając o tym, że nie sposób wyjaśnić znaczenia takich pojęć jak hydrofilowość i hydrofobowość. Hydrofilowość i hydrofobowość to cechy oddziaływania substancji i wody. Jeśli substancja i woda mają zbliżoną strukturę i silnie oddziałują ze sobą, na przykład tworzą wiązania wodorowe, to mówią o hydrofilowości. Przy słabym oddziaływaniu materii i wody mówią o hydrofobowości. Miarą intensywności oddziaływania międzycząsteczkowego jest napięcie powierzchniowe na granicy między substancją a wodą. Cząsteczki wody, posiadające duży moment dipolowy, silnie oddziałują ze sobą tworząc wiązania wodorowe. Nawet w parze wodnej w niskich temperaturach i umiarkowanych ciśnieniach znajduje się około 1% dimerów wody.
Woda jest doskonałym rozpuszczalnikiem. Dobrze rozpuszcza substancje polarne i dysocjujące na jony. Z punktu widzenia reaktywności woda jest substancją raczej obojętną. Ale niektóre substancje rozpuszczające się w wodzie reagują z nią. Tak więc gazy ΝΗ 3 i S0 2 rozpuszczające się w wodzie są przekształcane w jony NH 4 + i S0 3 2+.
Rozpuszczalniki organiczne
Woda jest najpowszechniejszym rozpuszczalnikiem nieorganicznym. Ale w środowisku rozpuszczalników organicznych nie ma pretendentów do wiodącej pozycji. Można jedynie wyróżnić grupę tak zwanych rozpuszczalników naftowych, które od niedawna nazywane są skrótem nefras. Jako rozpuszczalniki ropy naftowej stosuje się wąskie frakcje surowe lub frakcje wyizolowane z produktów wtórnej rafinacji ropy naftowej.
Większość rozpuszczalników pochodzenia naftowego ma historyczne nazwy, które często są zupełnie niezwiązane z ich składem i chemicznym charakterem związków wchodzących w ich skład. W niektórych przypadkach nazwy takich rozpuszczalników nie tylko nie informują, ale wręcz mylą użytkowników o ich składzie. Prawdziwym przykładem jest benzyna lakowa. Nieobciążony wiedzą języka angielskiego i staraj się naprawić „błąd” i nazwij go „białym duchem”. Do pewnego stopnia mają rację. Rzeczywiście, dosłownie przetłumaczony z angielskiego, biały spirytus oznacza „biały alkohol”. Ale ta nazwa najwyraźniej odzwierciedla tylko zewnętrzne podobieństwo. Skład chemiczny benzyny lakowej jest bardzo szeroki: węglowodory nasycone, węglowodory naftenowe, in mała ilość związki aromatyczne itp. Niestety, składnik alkoholowy jest nieobecny.
W celu uproszczenia i ujednolicenia nazw rozpuszczalników pochodzenia naftowego pojawiła się nazwa nefrasa. W zależności od składu węglowodorów nefras dzielą się na następujące typy:
- nefrasy C - rozpuszczalniki o mieszanym składzie, które zawierają węglowodory wszystkich klas;
- nefras A - rozpuszczalniki z przewagą węglowodorów alifatycznych i obniżoną zawartością węglowodorów aromatycznych (nie więcej niż 2,5%);
- nefras I - rozpuszczalniki z przewagą węglowodorów izoparafinowych;
- nefras P - rozpuszczalniki z przewagą węglowodorów parafinowych;
- nefras N - rozpuszczalniki z przewagą węglowodorów naftenowych;
- Ar nefras to rozpuszczalniki z przewagą węglowodorów aromatycznych.
Ponieważ nefras nie są indywidualnymi rozpuszczalnikami, nie mają ustalonej temperatury wrzenia. Gotują się w pewnym zakresie temperatur. Ten zakres jest również wskazany w ich nazwie.
Na przykład rozpuszczalnik zgodny z tą klasyfikacją nazywa się A 130/150. Oznacza to, że rozpuszczalnikiem jest mieszanina węglowodorów z przewagą związków alifatycznych i obniżoną zawartością związków aromatycznych, wrząca w zakresie temperatur od 130 do 150 °C.
W konwencjonalnym oznaczeniu benzyn rozpuszczalnikowych BR-1 (SZ 80/120) i BR-2 (C2 80/120) powszechnie stosowanych w produkcji sprzętu elektronicznego znajduje się jeszcze jedna cyfra. Faktem jest, że grupa mieszanych rozpuszczalników (C), w zależności od zawartości związków aromatycznych, dzieli się na podgrupy:
- 0 - mniej niż 0,1%;
- 1 - od 0,1% do 0,5%;
- 2 - od 0,5% do 2,5%;
- 3 - od 2,5% do 5,0%;
- 4 - od 5,0% do 25,0%;
- 5 - od 25,0% do 50,0%.
Mówią, że benzyny BR-1 i BR-2 są zamienne. Rzeczywiście, ich skład frakcyjny jest bliski. Ale jeśli te rozpuszczalniki są używane do mycia lub odtłuszczania czegoś, co jest nadmiernie wrażliwe na aktywne rozpuszczalniki, te ostatnie powinny być preferowane. Zawiera mniej węglowodorów aromatycznych. Co więcej, jest mniej toksyczny. Jeśli selektywność nie jest głównym wymogiem dla rozpuszczalnika, odpowiedź jest oczywiście inna.
Podobne myśli pojawiają się w związku z białym duchem. Rozpuszczalnik krajowy zawiera znacznie więcej związków aromatycznych niż jego zagraniczny odpowiednik (do 16%). Benzyna lakowa oczyszczona ze związków aromatycznych prawie nie ma zapachu, ale jego zdolność rozpuszczania jest znacznie mniejsza.
W przeciwieństwie do rozpuszczalników naftowych poszczególne rozpuszczalniki organiczne charakteryzują się stałymi ich właściwościami fizycznymi. Chociaż rozpuszczalniki techniczne mają również pewien zakres, w którym zmieniają się te właściwości. Ale ten zakres jest znacznie mniejszy niż w przypadku rozpuszczalników naftowych. Prawie wszystkie znane klasy są bogate w rozpuszczalniki. związki organiczne: węglowodory nasycone; chlorowane węglowodory; związki aromatyczne; alkohole; etery i estry; ketony itp. Właściwości fizyczne niektórych z najpopularniejszych rozpuszczalników organicznych przedstawiono w tabeli 1.
Termodynamika roztworów
Roztwory związków o niskiej masie cząsteczkowej i/lub o wysokiej masie cząsteczkowej są układami odwracalnymi. Są one zgodne z regułą faz Gibbsa i mogą być opisane za pomocą zwykłych diagramów stanów.
Rozpuszczanie jest procesem spontanicznym i towarzyszy mu spadek potencjału izobaryczno-izotermicznego (ΔG):
gdzie H- zmiana zawartości ciepła (entalpii) układu, S- zmiana entropii układu, T - temperatura bezwzględna, r- nacisk.
Rozpuszczalność związków chemicznych w rozpuszczalnikach określa powinowactwo termodynamiczne, którego miarą jest różnica między potencjałami izobaryczno-izotermicznymi roztworu a sumą potencjałów izobaryczno-izotermicznych składników:
Im większa wartość bezwzględna ΔG mieszaniny, im większe powinowactwo między składnikami, tym lepsza rozpuszczalność.
Jeśli zostawimy równania, to możemy powiedzieć, że podczas rozpuszczania dominuje zasada „podobne rozpuszcza się w podobnym”. Maksymalna wartość ΔG mieszaniny będzie w przypadku, gdy substancja rozpuszczona i rozpuszczalnik są do siebie jak najbardziej podobne. Z reguły substancje hydrofilowe lepiej rozpuszczają się w rozpuszczalnikach hydrofilowych, a substancje hydrofobowe lepiej rozpuszczają się w hydrofobowych. Dlatego próby rozpuszczenia kleju do tapet w benzynie zawsze będą skazane na niepowodzenie. Termodynamika temu się sprzeciwia.
Równowaga hydrofilowo-hydrofobowa
Kiedyś podszedł do mnie znajomy technolog, zdziwiony nielogicznym, jego zdaniem, zachowaniem lakieru melaminowo-alkidowego. Niespójność wyrażała się w tym, że konieczne było zmniejszenie jego lepkości, a on nie chciał się rozpuścić. Na pytanie, co próbowałeś rozpuścić, odpowiedź brzmiała: „Co jest zalecane na etykiecie – benzyna lakowa”. Jak upewnić się, że lakier nie chce się rozpuścić w tym, w czym musi się rozpuścić? Aby rozwiązać problem, nie musisz wymyślać niczego nowego. Rozwiązanie już istnieje, trzeba spróbować je wirtualnie powtórzyć, ograniczając się tylko do tego, że można korzystać tylko z wewnętrznych zasobów systemu.
Na pytanie, co zrobiłeś z tym lakierem, otrzymano odpowiedź: „Lakier był wcześniej używany do impregnacji transformatorów”. Obecność transformatorów w lakierze najprawdopodobniej nie mogłaby prowadzić do tak „poważnych” konsekwencji. Po wyjaśnieniu pytania okazało się, że chodzi o próżniową impregnację transformatorów. Na tym etapie przyczyna tak nieoczekiwanego zjawiska była dla mnie już w 90% jasna. A po tym, jak przyjrzałem się, jakie rozpuszczalniki były początkowo używane w lakierze, 90% już zamieniło się w 100%.
Cząsteczki spoiwa polimerowego (oligomerycznego) lakierów melaminowo-alkidowych zawierają fragmenty zarówno hydrofobowe, jak i hydrofilowe. Dlatego te lakiery wykorzystują mieszaninę rozpuszczalników (benzyna lakowa lub jej analogi oraz butanol). Pierwszy odpowiada za rozpuszczenie hydrofobowych fragmentów spoiwa, a drugi za rozpuszczenie hydrofilowych.
W normalnych warunkach odparowuje głównie bardziej lotny rozpuszczalnik. W tym przypadku benzyna lakowa lub jej analogi. Dlatego producenci zalecają, aby w przypadku zgęstnienia lakieru rozcieńczyć go benzyną lakową. Ale jeśli lakier zostanie wystawiony na działanie próżni, odparowuje również mniej lotny rozpuszczalnik, butanol. A dodawanie tylko benzyny lakowej nie wystarcza już do rozpuszczenia zagęszczonego lakieru. Grupy hydrofilowe lakieru wiążącego również wymagają rozpuszczalnika zbliżonego do nich pod względem chemicznym.
Podsumowując, możemy powiedzieć, że polimery lub oligomery (spoiwa dla większości farb i lakierów) zawierają fragmenty hydrofobowe i hydrofilowe w swoich łańcuchach molekularnych. Za właściwości hydrofobowe odpowiadają rodniki metylowe, etylowe i inne węglowodory. Hydroksylowe, karboksylowe i inne grupy polarne są hydrofilowe. W związku z tym rozpuszczalniki powinny również obejmować składniki o przeważających właściwościach hydrofobowych (benzyna lakowa, toluen, rozpuszczalnik itp.) oraz składniki wykazujące powinowactwo do wody (etanol, cellosolw etylowy, aceton, octan etylu itp.). A ich połączenie zależy od chemicznego charakteru lakieru wiążącego. Aby uzyskać niektóre lakiery, zestaw uniwersalnych „ponumerowanych” rozpuszczalników (tabela 2) jest niewystarczający. Dlatego musisz wymyślić własne unikalne kombinacje składników rozpuszczalnika. Równowaga hydrofilowo-hydrofobowa może być również realizowana w cząsteczkach jednego rozpuszczalnika.
Podobne problemy napotyka się w technologiach czyszczenia zespołów obwodów drukowanych z zanieczyszczeń. Ogólnie rzecz biorąc, te ostatnie różnią się również polarnością i odpowiednio hydrofilowością / hydrofobowością. W znanej mieszaninie alkohol-benzyna pierwszy składnik odpowiada za rozpuszczanie zanieczyszczeń hydrofilowych (przede wszystkim pozostałości kalafonii), a drugi za rozpuszczanie zanieczyszczeń hydrofobowych (tłuszcze itp.). W alkoholu izopropylowym (baza wielu obcych płynów myjących) równowaga hydrofilowo-hydrofobowa realizowana jest głównie w obrębie jednej cząsteczki.
Rozwiązania polimerowe
Roztwory polimerów i ich niskocząsteczkowych analogów (oligomerów) zainteresują głównie specjalistów zajmujących się nakładaniem powłok polimerowych i uszczelnianiem urządzeń radioelektronicznych materiałami polimerowymi.
Tabela 1. Właściwości fizyczne poszczególnych rozpuszczalników organicznych
Tabela 2. Skład niektórych „ponumerowanych” rozpuszczalników i rozcieńczalników
Roztwory polimerów mają szereg cech w porównaniu z roztworami związków niskocząsteczkowych ze względu na specyficzne właściwości makrocząsteczek: duże rozmiary, szeroki zakres elastyczności, duży zestaw konformacji (konfiguracji przestrzennych), możliwość zmiany konformacji wraz ze zmianą temperatury lub zmianą rozpuszczalnika itp. Roztwory polimerów charakteryzują się dużą lepkością, powolną dyfuzją, mają tiksotropię itp. Wszystko to z jednej strony komplikuje z nimi pracę, a z drugiej daje dużo więcej potencjalnych możliwości.
Cechą procesu rozpuszczania związków wielkocząsteczkowych jest ich pęcznienie. Szybkość dyfuzji makrocząsteczek jest znacznie niższa niż szybkość dyfuzji cząsteczek rozpuszczalnika. Dlatego te ostatnie szybciej wnikają w fazę polimeru niż makrocząsteczki do rozpuszczalnika. W rezultacie znacznie zwiększa się objętość polimeru. Obrzęk nie zawsze może skutkować rozpuszczeniem. Jeżeli polimer i rozpuszczalnik są zmieszane ze sobą w ograniczonym stopniu, na końcu procesu powstają dwie fazy: nasycony roztwór polimeru w rozpuszczalniku i nasycony roztwór rozpuszczalnika w polimerze. Wraz ze zmianą warunków, na przykład temperatury, ograniczone rozpuszczanie może zmienić się w nieograniczone i odwrotnie.
Polimery o strukturze przestrzennej (trójwymiarowej) w najlepszy przypadek może tylko puchnąć. Obecność wiązań chemicznych nie pozwala makrocząsteczkom oderwać się od siebie i przejść do roztworu.
W praktyce, przygotowując roztwory polimerów, bierze się pod uwagę specyfikę ich rozpuszczania, bez jednoczesnego wprowadzania do roztworu całego rozpuszczalnika. W przeciwnym razie na powierzchni polimeru tworzy się spuchnięta otoczka, uniemożliwiająca dalsze przenikanie rozpuszczalnika. Myślę, że taki problem napotkali ci, którzy próbowali za jednym razem przygotować kleje do tapet na bazie skrobi, karboksymetylocelulozy i innych polimerów rozpuszczalnych w wodzie.
Równowagę fazową w układzie „polimer – rozpuszczalnik” określa reguła fazowa Gibbsa:
gdzie C to liczba stopni swobody w układzie, K to liczba komponentów, a Ф to liczba faz.
Reguła fazy określa stan układu w momencie równowagi, niezależnie od drogi, po której układ zbliżył się do tego stanu. Liczba stopni swobody C wskazuje, ile zmiennych określających stan układu można dowolnie zmieniać bez zmiany liczby faz.
Z tego równania wynika, że w układach dwuskładnikowych maksymalna liczba stopni swobody wynosi trzy. Oznacza to, że stan układu „polimer – rozpuszczalnik” jest całkowicie determinowany przez temperaturę, ciśnienie i stężenie polimeru. Ponieważ w układach skondensowanych równowaga jest prawie niezależna od ciśnienia, dlatego regułę fazową można zapisać w uproszczonej formie:
System jednofazowy ma dwa stopnie swobody. W dwóch fazach system ma tylko jeden stopień swobody. Oznacza to, że zmiana temperatury automatycznie prowadzi do zmiany stężenia w obu fazach.
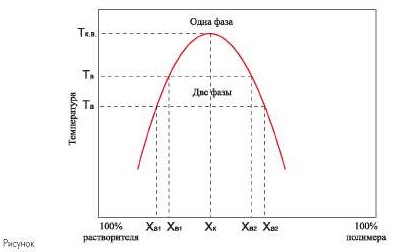
Rysunek przedstawia typową krzywą równowagi fazowej w dwuskładnikowym układzie polimer-rozpuszczalnik.
Krzywa równowagi fazowej oddziela obszar nieograniczonego rozpuszczania od obszaru ograniczonego rozpuszczania.
W obszarze ograniczonego rozpuszczania, na przykład w punkcie „a”, liczba faz wynosi 2, a liczba stopni swobody wynosi 1. Stan układu jest jednoznacznie określony przez temperaturę lub stężenie. W punkcie „a” roztwór polimeru charakteryzuje się temperaturą Ta i składem faz: faza 1 – x a1 i faza 2 – x a2. Wraz ze wzrostem temperatury stężenia roztworów w obu fazach zaczynają się zbiegać, a także zmieniają się objętości faz. Po osiągnięciu temperatury Tq (górny krytyczny) składy obu faz wyrównują się i następuje przejście z układu dwufazowego do jednofazowego - jednorodny roztwór polimeru w rozpuszczalniku. Schłodzenie układu jednofazowego spowoduje ponowne rozwarstwienie. To przejście można wykonać nieograniczoną liczbę razy.
Diagramy fazowe dla rzeczywistych układów polimer-rozpuszczalnik nie są takie proste. Nie ma ostrej granicy między obszarami nieograniczonego i ograniczonego rozwiązania. Ze względu na polidyspersyjność polimerów krzywa równowagi fazowej jest praktycznie zbiorem krzywych odpowiadających poszczególnym frakcjom polimeru. Separacja faz w roztworach polimerów może następować nie tylko wraz ze spadkiem, ale także ze wzrostem temperatury.
W przeciwieństwie do roztworów związków o niskiej masie cząsteczkowej, roztwory polimerów, nawet w bardzo niskich stężeniach, są raczej lepkimi mediami. Ale to nie jest główna różnica. Zdolność cząsteczek polimeru do odkształcania się pod wpływem zewnętrznego pola siłowego i orientowania się w przepływie prowadzi do tego, że lepkość staje się zmienna.
Przepływ cieczy o małej masie cząsteczkowej i ich roztworów jest zgodny z prawem Newtona:
gdzie τ jest naprężeniem ścinającym, Pa; η - współczynnik lepkości, Pa • s; γ - szybkość ścinania (gradient szybkości ścinania), s -1.
W płynach newtonowskich lepkość η nie zależy od naprężenia ścinającego (szybkości). W układach strukturalnych w większości przypadków lepkość zależy od naprężenia ścinającego. Roztwory polimerowe są na ogół cieczami nienewtonowskimi. Ich lepkość spada wraz ze wzrostem gradientu prędkości. Im szybciej taka ciecz płynie, tym mniejsza jest jej lepkość. Wyjaśnienie jest bardzo proste. Przy niskich stężeniach poszczególne makrocząsteczki są zorientowane wzdłuż przepływu. W obszarze wysokich stężeń struktury powstające podczas wzajemnego oddziaływania makrocząsteczek ulegają zniszczeniu. Przy bardzo małych lub bardzo wysokich natężeniach przepływu roztwory polimerów również podlegają prawu Newtona.
Efektywna lepkość roztworów polimeru zależy od stężenia, masy cząsteczkowej polimeru, rozkładu masy cząsteczkowej, temperatury i charakteru rozpuszczalnika.
Znane są różne typy lepkości: kinematyczna, dynamiczna, względna, specyficzna, zredukowana, a dla polimerów także charakterystyczna. Lepkość istotna to zmniejszona lepkość ekstrapolowana do zerowego stężenia polimeru.
W praktyce lepkość polimerów najczęściej ocenia się mierząc nie wartości bezwzględne, ale czas przepływu płynu przez kalibrowany otwór. W produkcji farb i lakierów technolodzy zwykle operują tzw. lepkością według VZ-4. Pomiar takiej lepkości sprowadza się do pomiaru czasu ważności (w sekundach) określonej objętości materiału farby i lakieru ze zwykłego lejka przez skalibrowany otwór. Ponieważ technologia nakładania powłok malarskich i lakierniczych pozwala na zmianę lepkości w dość szerokim zakresie, dokładność takiego pomiaru jest wystarczająca. W przypadku farb i lakierów o wysokiej lepkości stosuje się podgrzewane lejki.
Dokładniejsze pomiary przeprowadza się za pomocą termostatowania na lepkościomierzu kapilarnym, na przykład VPZh-1, VPZh-2, VPZh-4. W takim przypadku możliwe staje się przejście od sekund do Wartości bezwzględne lepkość.
Rozwiązania odwrotne
Większość praktycznie stosowanych polimerów w czystej postaci nie ma właściwości wysoce elastycznych. Takie właściwości mogą pojawić się po dodaniu specjalnych związków niskocząsteczkowych,
zwane plastyfikatorami. Układ „polimer – plastyfikator” w rzeczywistości jest bardzo stężonym roztworem, w którym zawartość plastyfikatora waha się od ułamków procentowych do kilkudziesięciu procent. Są to rozwiązania o przeciwnym znaku - roztwór cieczy w ciele stałym (roztwór stały).
Plastyfikować można prawie wszystkie polimery. Aby zapewnić wymagany zestaw właściwości eksploatacyjnych, układ „polimer - plastyfikator” musi długo zachowywać swoje właściwości. Osiąga się to poprzez użycie substancji jako plastyfikatorów, które mają wysoka temperatura temperatura wrzenia i bardzo niska lotność.
Plastyfikatory są klasyfikowane według ich charakteru chemicznego i stopnia kompatybilności z polimerem. Po raz pierwszy jako plastyfikator zastosowano kamforę, a pierwszym plastyfikowanym tworzywem sztucznym był celuloid (Anglia, II poł. XIX w.). Obecnie najszerzej stosowanymi plastyfikatorami są estry kwasu ftalowego (około 80% całkowitej objętości). Stosowane są również estry alifatycznych kwasów dikarboksylowych, estry kwasu fosforowego, poliestry o niskiej masie cząsteczkowej, chlorowane parafiny, ciecze krzemoorganiczne, parafiny, produkty chemiczne drewna itp.
Istotą plastyfikacji jest zwiększenie elastyczności i ruchliwości makrocząsteczek w obecności składnika o niskiej masie cząsteczkowej. Z reguły nieodzownym warunkiem plastyfikacji jest termodynamiczna zgodność plastyfikatora z polimerem, czyli utworzenie w polimerze prawdziwego roztworu plastyfikatora. Gdy stosuje się plastyfikator o powinowactwie termodynamicznym do polimeru, następuje samorzutne tworzenie się jego prawdziwego roztworu w polimerze (polimer pęcznieje w plastyfikatorze).
Jeśli plastyfikator nie ma powinowactwa do polimeru, jego wprowadzenie do polimeru można przeprowadzić na siłę - w mieszalnikach. W tym przypadku powstaje termodynamicznie niestabilny układ koloidalny, podatny na rozwarstwienie. Zewnętrznie objawia się to pojawieniem się kropelek plastyfikatora na powierzchni produktu. Dzięki udanej kombinacji „polimer - plastyfikator” takie procesy zachodzą bardzo wolno, w wyniku czego produkty zachowują swoje właściwości eksploatacyjne przez kilkadziesiąt lat.
Ze względu na charakter interakcji z polimerami plastyfikatory można podzielić na dwie grupy: polarną i niepolarną. Te pierwsze są zdolne do solwatowania grup polarnych polimeru, zmniejszając ich oddziaływanie międzycząsteczkowe, a w konsekwencji temperaturę zeszklenia. Spadek temperatury zeszklenia jest proporcjonalny do liczby moli wprowadzonego plastyfikatora (reguła Żurkowa). Plastyfikatory niepolarne nie zmieniają znacząco energii wewnętrznej układu. Pełnią rolę swego rodzaju smaru. Dlatego są inaczej nazywane zmiękczaczami.
Szczególnym rodzajem plastyfikacji jest uplastycznienie polimeru polimerem. Elastyczność sztywnego polimeru można zwiększyć, dodając do niego polimer elastyczny. Warunek wymagany- powinowactwo termodynamiczne polimerów. Przykład takiego termodynamicznie stabilnego układu: „polichlorek winylu – kauczuk butadienowo-nitrylowy”.
Aspiracje wodne
Istnieją związki chemiczne zwane izocyjanianami. Izocyjaniany zawierają grupy funkcyjne -NCO. Są to niezwykle reaktywne i toksyczne związki. Wysoka aktywność chemiczna i wysoka toksyczność z reguły współistnieją ze sobą. W produkcji sprzętu elektronicznego izocyjaniany są stosowane jako utwardzacz lakieru alkidowo-uretanowego UR-231 - dietylenoglikoluretanu (DGU), przy produkcji związków itp.
Wysoka aktywność chemiczna znalezisk izocyjanianów praktyczne użycie oraz w innych obszarach. Tak więc do modyfikacji poliolefin diizocyjanianami zsyntetyzowano związek chemiczny o bardzo długiej nazwie: 1,1-1,6-heksametyleno-3,3,3 1,3-tetrakis-(2-hydroksyetylo)-bisurea (dalej - bisurea ). Dodatek powstał w wyniku oddziaływania 1,6-heksametylenodiizocyjanianu i dietanoloaminy zgodnie z reakcją:
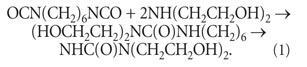
Suplement ten przypadkowo trafił w ręce lekarzy. Okazało się, że posiada wyjątkowe właściwości krioochronne. Już ze szkolnego kursu fizyki wiemy, że w przeciwieństwie do większości związków chemicznych, woda nie zmniejsza objętości, gdy zamarza, lecz zwiększa się. To dzięki temu lód nie tonie, ale unosi się. To dzięki temu życie utrzymuje się w zbiornikach itp. Z drugiej strony, dzięki tej samej właściwości wody, gdy jakakolwiek żywa istota zamarza, kryształki lodu nieodwracalnie niszczą komórki organiczne. Ale przedmioty biologiczne (krew, szpik kostny, narządy ludzkie itp.) Można zachować przez długi czas, zamrażając je w temperaturze ciekłego azotu (-196 ° C) w obecności krioprotektantów. W praktyce najczęściej stosuje się do tego dimetylosulfotlenek, związek raczej toksyczny i niewystarczająco skuteczny. Okazało się, że bisurea ma doskonałe właściwości krioochronne. A co najważniejsze, pomimo ekstremalnej toksyczności związków chemicznych użytych do jej otrzymania, sam w sobie jest praktycznie nietoksyczny. Według twórców można go nawet rozsmarować na chlebie i zjeść.
Po pozytywnych wynikach testów pojawiła się potrzeba opracowania przemysłowej technologii produkcji bimocznika. Początkowo syntezę dodatku prowadzono zgodnie z reakcją (1) przy użyciu tradycyjnej dla chemii technologii - w rozpuszczalniku organicznym. Produkt docelowy otrzymano w postaci roztworu i wyizolowano w postaci krystalicznej znanymi metodami, na przykład wielokrotną rekrystalizacją. Technologia jest złożona i wieloetapowa, szczególnie na etapie oczyszczania bismocznika z zanieczyszczeń. Chemicy zwykle odchodzą od rozpuszczalników organicznych, jeśli to możliwe. Deweloperzy je zostawili, zastępując rozpuszczalnik organiczny zwykłą wodą. Rozwiązanie jest super oryginalne. Faktem jest, że początkowy produkt (diizocyjanian) aktywnie reaguje z wodą. Zaproponowano prowadzenie reakcji w bardzo niskiej (ujemnej) temperaturze. W tej temperaturze reakcja (1) nadal zachodzi, a szybkość reakcji diizocyjanianu z wodą praktycznie spada do zera. Wybierając to rozwiązanie, twórcy mieli na uwadze, że nawet w normalnej temperaturze szybkość reakcji (1) była kilkakrotnie wyższa niż szybkość reakcji diizocyjanianu z wodą. Produkt docelowy uzyskano w postaci roztworu wodnego i właśnie w tej postaci był stosowany w medycynie. W konsekwencji zniknęła potrzeba oddzielania bimocznika od roztworu. W teorii, a w niektórych przypadkach w praktyce, wszystko układało się świetnie. Ale jakoś roztwór wodny Bimoczniki otrzymywane tą technologią często okazywały się toksyczne.
Na tym etapie autor dołączył do twórców technologii. Oddając hołd pięknu rozwiązania technicznego, możemy powiedzieć, że nie obyło się bez wad. Główną wadą tej technologii było to, że była wydajna tylko wtedy, gdy początkowe produkty reakcji (1) były przyjmowane w absolutnie stechiometrycznych proporcjach. Teoretycznie jest to możliwe, ale w praktyce możemy tylko mniej lub bardziej się do tego zbliżyć. Przypomnę, że 1 g-mol substancji zawiera 6,02 · 10 23 cząsteczek (liczba Avogadro). Postaraj się wprowadzić substancje do reakcji z taką precyzją, aby każdej cząsteczce jednej substancji dokładnie odpowiadała ta sama liczba cząsteczek innej substancji (w tym przypadku stosunek wynosi 2:1). Jest mało prawdopodobne, że się to uda. Dlatego w przypadkach, gdy stosunek składników wyjściowych w reakcji był bliski stechiometrycznemu, otrzymano nietoksyczny produkt. W innych sytuacjach, zgodnie z teorią prawdopodobieństwa, powinny one zdarzać się znacznie częściej, roztwór okazał się toksyczny ze względu na pozostałości toksycznych związków wyjściowych.
Do rozwiązania tego pozornie nierozwiązywalnego problemu wykorzystano znaną z teorii rozwiązywania problemów wynalazczych (TRIZ) technikę rozwiązywania technicznych sprzeczności (za pomocą częściowo nadmiarowego lub częściowo brakującego działania). Jedna substancja z materiału wyjściowego (diizocyjanian) została pobrana nieco więcej niż jest to konieczne do reakcji. Roszczenia, w których zaimplementowano to rozwiązanie, są następujące:
Sposób otrzymywania 1,1-1,6-heksametyleno-3,3,3 1,3-tetrakis-(2-hydroksyetylo)-bismocznika przez oddziaływanie 1,6-heksametylenodiizocyjanianu z dietanoloaminą w środowisku rozpuszczalnika, następnie zatrzymanie mieszaniny reakcyjnej i wyodrębnienie produktu docelowego, charakteryzującego się tym, że diizocyjanian heksametylenu pobiera się w ilości 1.0005-1,1 ze stanu stechiometrycznego, a jako rozpuszczalnik stosuje się wodę i mieszaninę reakcyjną utrzymuje się w temperaturze 25-60°C przez czas potrzebny do wytworzenia 1,6-heksametylenodiizocyjanianu.
Nadmiar w stosunku do stechiometrycznej ilości zocyjanianu 1,6-hesametylenodiu gwarantuje we wszystkich przypadkach nieobecność dietanoloaminy w wodnym roztworze produktu docelowego. Pozostający w środowisku reakcji 1,6-heksametylenodiizocyjanian jest przekształcany w polimoczniki podczas późniejszej ekspozycji w wyniku reakcji z rozpuszczalnikiem (wodą). Polimoczniki wytrącają się i są odfiltrowywane. W ten sposób otrzymuje się wodny roztwór bismocznika, gotowy do użycia zgodnie z przeznaczeniem. Iniekcje takiego mysiego roztworu, na którym testowano jego toksyczność, były tolerowane bezboleśnie. W ten oryginalny sposób praktycznie zrealizowano „wodne aspiracje” w tej technologii.
„Aspiracje wodne” można prześledzić w prawie wszystkich technologiach produkcji sprzętu elektronicznego. W niektórych technologiach (galwanizacja lub powlekanie chemiczne, trawienie itp.) ich wdrożenie nie wymaga wysiłku. Zasadniczo do uzyskania takich powłok można również stosować media niewodne. Trwają badania naukowe w tym kierunku. Ale czy to naprawdę konieczne?
W innych technologiach, na przykład przy tworzeniu pośrednich lub wykończeniowych powłok płytek obwodów drukowanych (fotomaski, maski lutownicze), trzeba było poczynić znaczne wysiłki, aby odejść od kompozycji opracowanych organicznie na rzecz wodno-alkalicznych.
Tendencja do odchodzenia od „materii organicznej” dominuje również w technologiach czyszczenia zespołów obwodów drukowanych z wszelkiego rodzaju zanieczyszczeń. Detergenty na bazie wody zastępują toksyczne i nieprzyjazne dla środowiska rozpuszczalniki organiczne.
Ciąg dalszy nastąpi.
Literatura
- Słownik politechniczny / Redakcja .: A. Yu Ishlinsky i in. M .: Sov. Encyklopedia. 1989.
- Encyklopedia chemiczna: W 5 tomach Vol. 1 / Redakcja: I. L. Knunyants i wsp. M.: Sov. Encyklika, 1988.
- Salem L. Cudowna cząsteczka // Per. z francuskiego M: Mir, 1982.
- GOST 8420-74. Farby i lakiery. Metody określania lepkości warunkowej.
- Musakin A.P., Rachinsky F. Yu., Suglobova KD Sprzęt do laboratoriów chemicznych. L .: Chemia, 1982.
- Barshtein R. S, Kirilovich V. P., Nosovskiy Yu. E. Plastyfikatory do materiałów polimerowych. Moskwa: Chemia, 1982.
- Sondy J. H., Frisch K. K. Chemia poliuretanów // Przeł. z angielskiego. Moskwa: Chemia, 1972.
- Poklepać. RF № 2072352. Urazaev VG, Arkhireev VP, Batdalov Yu R. Sposób otrzymywania ^ - ^ 6-heksametyleno-ZDZ ^ 3`-tetra-kis (2-hydroksyetylo) -bisurea. Priorytet od 10.08.1994.
Rozpuszczalniki organiczne są szeroko poszukiwane w przemyśle chemicznym, budowlanym, remontowym, produkcji farb i lakierów, motoryzacji, poligrafii itp. Służą do rozszczepiania tłuszczów, przygotowywania klejów i impregnatów, usuwania zabrudzeń i osadów. Artykuł skupi się na różnorodności i prawidłowe użycie rozpuszczalniki organiczne.
Rozpuszczalniki organiczne
Cechą substancji jest ich organiczny charakter i zdolność rozpuszczania związków różnego typu. Zgodnie z metodą ich otrzymywania wyróżnia się takie główne grupy, jak:
- węglowodory;
- ketony;
- etery i estry;
- alkohole;
- rozpuszczalniki chlorowcowane.
Gęstość rozpuszczalników organicznych zależy od temperatury.
Zdjęcie materii organicznej rozpuszczalnika

Stosowanie rozpuszczalników organicznych
- Ciecze rozpuszczające i ich homologi są szeroko stosowane w wielu dziedzinach przemysłu. Są również poszukiwani na prace restauracyjne i restauracyjne wartości artystycznych. Służą do przygotowania impregnatów, lakierów i czyszczenia przedmiotów z dowolnych materiałów.
- W fabrykach samochodowych i warsztatach naprawczych używa się głównie benzyny, ksylenu, węglowodorów chlorowanych, benzyny lakowej i nafty. Z ich pomocą odbywa się mycie, moczenie, mycie i odtłuszczanie części maszyn.

Produkcji farb i lakierów nie można sobie wyobrazić bez rozpuszczalników organicznych, które w większości stanowią podstawę do wytwarzania szeregu produktów.
W życiu codziennym rozpuszczalniki są potrzebne w następujących przypadkach:
- do rozcieńczania silnie skoncentrowanych materiałów lakierniczych do wymaganej konsystencji, lepkości;
- do usuwania plam z materiałów barwiących z ubrań lub powierzchni;
- do czyszczenia narzędzia roboczego, które było używane podczas malowania (pędzel, pistolet natryskowy, wałek itp.).
Skuteczne czyszczenie osadów lub zabrudzeń zależy od prawidłowego doboru odpowiedniego rozpuszczalnika. W poniższej tabeli przedstawiono najczęstsze przykłady usuwania zwisów o różnym charakterze.
Cieńszy czy cieńszy
- Wiele osób używa tych słów jako synonimów. ale skład chemiczny rozpuszczalniki organiczne mają zupełnie inne właściwości fizyczne i techniczne. Dodanie rozcieńczalnika do stężonych materiałów nie pociąga za sobą żadnej reakcji.
- Z kolei rozpuszczalnik działa na substancję, wnikając w jej strukturę, rozpuszcza składniki błonotwórcze. W ten sposób farby, lakiery emaliowane uzyskują optymalną płynność (lepkość) do barwienia.

Stosowane rozpuszczalniki muszą spełniać 2 podstawowe wymagania:
- zdolność do przekształcania substancji błonotwórczych w stan ciekły;
- podczas parowania zapewniają optymalną strukturę powłoki, bez utraty pierwotnych właściwości i bez powstawania defektów na malowanej powierzchni.
Rodzaje rozpuszczalników organicznych
Rozpuszczalniki organiczne to często substancje płynne o charakterystycznym ostrym zapachu. Klasyfikacja odbywa się na podstawie budowy chemicznej, właściwości fizycznych i innych parametrów, które określają ich zdolność do interakcji z różnymi substancjami.
Według składu:
- związki jednorodne to alkohol butylowy, aceton, rozpuszczalnik, benzyna, izopropanol;
- substancje wieloskładnikowe (połączone) - P646, 649, P-4 itp.
Szybkość parowania:
- do emalii i lakierów stosuje się substancje o niskiej lotności (terpentyna);
- jako rozcieńczalniki do farb olejnych stosuje się rozpuszczalniki o średniej lotności (nafta);
- wysoce lotne rozpuszczalniki organiczne (benzyna, benzyna lakowa) nadają się do prawie wszystkich rodzajów farb i lakierów.
Należy pamiętać, że im większy stopień lotności, tym większa ich wybuchowość i palność.
Temperatura wrzenia:
- niskowrzący - do 100 stopni;
- średnie gotowanie - do 150 stopni;
- wysokie wrzenie - ponad 150 stopni.
Praca z rozpuszczalnikami organicznymi
W zależności od rodzaju rozpuszczalnika, czyli jego gęstości, aplikację można przeprowadzić w następujący sposób:
- metoda pędzla;

- zanurzenie;
- wylewanie strumieniem;
- narażenie w oparach substancji;
- natryskiwanie pneumatyczne, bezpowietrzne lub elektrostatyczne;
- elektroosadzanie.
Przegląd popularnych rozpuszczalników organicznych
Rozpuszczalniki organiczne są aktywnie wykorzystywane w przestrzeni poradzieckiej ze względu na ich wysoką odporność na trudne warunki klimatyczne.
Grupa węglowodorowa
Benzyna „Galosha”, Nefras
- Substancje te są otrzymywane podczas destylacji oleju o niskiej zawartości siarki. Są przezroczystą cieczą (dopuszcza się żółtawy odcień) o słodkawym zapachu. Główną różnicą między prezentowanymi produktami są wyraźne właściwości rozpuszczania farb i emalii.
- Służą do rozcieńczania materiałów lakierniczych, przygotowywania i czyszczenia powierzchni. Te silne rozpuszczalniki są pożądane w biżuterii, gdzie wymagane są wysokie wyniki przy minimalnych dawkach.
Terpentyna
- Bezbarwna i łatwopalna ciecz - wynik destylacji drewna sosnowego lub destylacji żywicy drzewa iglaste(terpentyna gumowa). Jego temperatura zapłonu wynosi 34 stopnie.
- Rozpuszczalnik o ostrym zapachu służy do rozcieńczania farb olejnych i alkidowych, lakierów, a także do czyszczenia narzędzi. Idealnie nadaje się do odtłuszczania powierzchni przed malowaniem lub klejeniem.

Biały duch
- Przez zmieszanie węglowodorów alifatycznych i aromatycznych uzyskuje się płynną przezroczystą substancję o ostrym specyficznym zapachu. Substancja bardzo skutecznie odtłuszcza powierzchnie i usuwa zanieczyszczenia olejowe.
- Ponadto jest stosowany jako rozcieńczalnik do emalii alkidowych, lakierów, mas bitumicznych lub gumowych. Kompozyt rozpuści tłuszcze, frakcje ropy naftowej, organiczne związki tlenu, azotu itp.
Ksylen
- Ten aromatyczny węglowodór jest bezbarwną cieczą bez zanieczyszczeń. Przyjemny zapach nie powinien wprowadzać w błąd, wysokie stężenie oparów na pewno zaszkodzi zdrowiu.
- Z łatwością radzi sobie z takimi zadaniami funkcjonalnymi jak: rozpuszczanie farb na bazie żywic epoksydowych, lakierów polimerowych, mas poliuretanowych. Niskie parowanie zapewnia gładszą i bardziej błyszczącą powierzchnię.
Grupa ketonów
Aceton
- Bezbarwna, lotna ciecz o ostrym zapachu jest wysoce łatwopalna. Otrzymywany jest w procesie syntezy fenolu. Wyróżnia się korzystnie dobrym mieszaniem z wodą i innymi podobnymi rozpuszczalnikami.
- Jest szeroko stosowany do rozpuszczania emalii nitro i lakierów nitro, a także niektórych soli: jodku potasu, chlorku wapnia. Rozbija tłuszcze na powierzchniach gumowych, usuwa tłuste i woskowe plamy.

Keton metylowo-izobutylowy
- Ten rozpuszczalnik jest bezbarwny i ma ostry, słodkawy zapach. Jest wynikiem kondensacji acetonu z dalszym odwodnieniem i uwodornieniem tlenku mezytylu.
- Jest aktywnie wykorzystywany jako ważny składnik w produkcji farb na bazie żywic epoksydowych. Doskonale rozpuszcza kalafonię, gumę, kopolimer chlorku winylu, wiele żywic naturalnych i syntetycznych.
Cykloheksanon
- Lekko lepka bezbarwna ciecz ma bardzo ostry zapach o miętowym odcieniu. Substancja wysoce łatwopalna zbliżona właściwościami do acetonu. Otrzymywany jest przez utlenianie cykloheksanu w obecności naftenianu.
- Niezastąpiony do rozpuszczania azotanów, żywic naturalnych, olejów, octanów celulozy, polichlorków winylu. Wraz z octanem etylu nadaje się do rozcieńczania większości rodzajów farb. On jest część odplamiacze.
Grupa eterów i estrów
Dioksan 1,4
- To syntetyczny eter. Jest bezbarwną cieczą o silnym zapachu. Łatwo rozpuszczalny w wodzie, alkoholu i mieszalny z eterami.
- Szczególnie poszukiwany w produkcji lakierów nitro i octanu celulozy. Jest stosowany jako rozpuszczalnik do farb. Swobodnie rozkłada tłuszcze, oleje, woski itp. Nadaje się jako stabilizator rozpuszczalników chlorowanych.
Octan etylu
- Bezbarwny ester ma przyjemny zapach (w niskich stężeniach). Otrzymywanie odbywa się w wyniku przetwarzania syntetycznego kwasu octowego. Ciecz palna charakteryzuje się wysoką rozpuszczalnością i lotnością.
- Służy do czyszczenia i odtłuszczania powierzchni, a także rozpuszczania folii, eterów celulozy, pigmentów, farb olejnych, lakierów poliestrowych, emalii, olejów smarnych.
Octan metylu
- Bezbarwny octan etylu służy do rozpuszczania eterów celulozy, większości rodzajów żywic, tłuszczów, farb i lakierów. Można go łączyć z innymi rozpuszczalnikami.
- Pod względem właściwości rozpuszczających jest podobny do acetonu i z powodzeniem może być stosowany jako jego zamiennik. Jednak octan metylu jest wysoce toksyczny pomimo przyjemnego zapachu.
Grupa alkoholowa
Etanol
- Dzięki beztlenowej fermentacji węglowodorów roślinnych uzyskuje się łatwo mobilną ciecz o charakterystycznym zapachu. Łatwopalny w kontakcie z ogniem.
- Alkohol przemysłowy wykorzystywany jest do produkcji farb i lakierów. Są szeroko stosowane do dezynfekcji i odtłuszczania powierzchni przed dalszym malowaniem lub klejeniem.

Metanol
- Bezbarwny alkohol jednowodorotlenowy jest wysoce łatwopalny i ma charakterystyczny zapach. Pozyskiwany jest w sposób syntetyczny. Łatwo mieszalny z wodą i większością rozpuszczalników organicznych (etanol, aceton, benzen).
- Znalazł szerokie zastosowanie w produkcji materiałów lakierniczych. Ze względu na wysoką toksyczność stosowanie metanolu w wielu produktach konsumenckich jest zabronione.
Butanol
- Lekko lepka ciecz nie ma koloru, ale ma charakterystyczny zapach fuzlu. Jego produkcja oparta jest na procesie oksosyntezy z aldehydu octowego. Jest ważnym składnikiem w produkcji materiałów lakierniczych, plastyfikatorów i żywic.
- Właściwości chemiczne rozpuszczalników organicznych pozwalają na rozpuszczanie schnących olejów, lakierów, farb, gum, żywic naturalnych i syntetycznych. Nadaje się do usuwania osadów i zabrudzeń różnego pochodzenia.
Zasady pracy z rozpuszczalnikami organicznymi
Większość rozpuszczalników organicznych ma negatywny wpływ na zdrowie człowieka. Dotkliwość wpływu zależy od ich rodzaju. Aby wykluczyć zatrucie lub przynajmniej zmniejszyć efekt toksyczny, podczas pracy z nimi należy przestrzegać zasad bezpieczeństwa.
- Stosowanie środków ochrony osobistej, czyli nie zaniedbuj okularów, rękawiczek, masek oddechowych.

- W przypadku kontaktu ze skórą natychmiast wytrzeć suchą, czystą szmatką i spłukać pod bieżącą wodą.
- Przestrzeń przeznaczona do pracy musi być wyposażona w system wentylacji. W ostateczności otwierają się okna i drzwi wejściowe.
- Ważne jest, aby monitorować temperaturę w skrzyni roboczej, niektóre rozpuszczalniki są wybuchowe. W związku z tym zabronione jest używanie ich w bezpośrednim sąsiedztwie gorących (żarowych) przedmiotów.
- Pojemniki z rozpuszczalnikami organicznymi są transportowane i przechowywane w chłodnych pomieszczeniach w pozycji ściśle pionowej (szyja do góry).
Bezpieczeństwo i zdrowie
Zdolność do rozpuszczania się w tłuszczach oraz lotność rozpuszczalników organicznych odpowiadają za ich toksyczny wpływ na zdrowie człowieka. Zwykle negatywne skutki występują przez drogi oddechowe i skórę.
- Zatrucie objawia się następującymi objawami: podrażnieniem skóry, błony śluzowej dróg oddechowych i układu pokarmowego. W ostrej toksyczności mogą wystąpić szumy uszne, nudności, pobudzenie, drętwienie opuszków palców, pocenie się i nieregularne bicie serca.
- W warunkach pracy, w których z reguły dochodzi do długotrwałego kontaktu z substancjami o niskim stężeniu, pracownicy rozwijają przewlekłe zatrucia. Towarzyszy mu słaby apetyt, zmęczenie, senność i utrata wagi.
Specyficzne działanie rozpuszczalników organicznych może objawiać się dowolnymi znakami, a także ich kombinacjami.
- Aromatyczne węglowodory powodować podrażnienie ośrodkowego układu nerwowego, zmianę obrazu krwi. Na skórze może pojawić się zaczerwienienie, któremu towarzyszy swędzenie.
W pomieszczeniach roboczych stężenie par benzenu w powietrzu nie powinno przekraczać 5 mg/m3, dla toluenu i ksylenu - 50 mg/m3.
- Węglowodory tłuszczowe... Obejmuje to popularne rozpuszczalniki, takie jak benzyna, eter naftowy i benzyna lakowa. W przewlekłym zatruciu obserwuje się niestabilność psychiczną, drżenie powiek i wyciągnięte ramiona. Obecność chloru w węglowodorach tłuszczowych (substancjach podstawionych chlorem) wywiera specyficzny wpływ na narządy wewnętrzne, rozwija anemię i zaburza czynność serca.

W przypadku pomieszczeń roboczych stężenie oparów w powietrzu dla mieszaniny węglowodorów alifatycznych i aromatycznych nie powinno przekraczać 100 mg/m3, dla czterochlorku węgla - do 2 mg/m3, dichloroetanu - 10 mg/m3. młode.
- Alkohole dostać się do organizmu przez drogi oddechowe lub skórę. Atomy węgla powoli gromadzą się w organizmie i są wydalane jeszcze wolniej. Typowe objawy zatrucia to: bóle głowy, zanik nerwu wzrokowego, a także przewlekła choroba nerek i serca.
W pomieszczeniach roboczych stężenie metanolu w powietrzu nie powinno przekraczać 5 mg/m3, dla alkoholu propylowego i butylowego - 10 mg/m3.
- estry renderowanie silny wpływ na zdrowie ludzkie. Przy długotrwałej inhalacji pojawiają się bóle głowy, przyspieszone tętno, pogorszenie widzenia, podrażnienie błon śluzowych oczu.
W przypadku pomieszczeń roboczych stężenie par estrów w powietrzu nie powinno przekraczać 100 mg/m3.
- Ketony Popularnym rozpuszczalnikiem w tej grupie jest aceton. Jego wysokie stężenie prowadzi do ostrego zatrucia, którego objawami są anemia, podrażnienie błon śluzowych, zawroty głowy, łzawienie.

W przypadku pomieszczeń roboczych stężenie par ketonów w powietrzu nie powinno przekraczać 200 mg/m3.
- Dwusiarczek węgla jest substancją wysoce toksyczną. W ciężkim zatruciu obserwuje się zaburzenia psychiczne, zaburzenia przewodu pokarmowego, upośledzenie pamięci, drżenie rąk i utratę wzroku.
W przypadku pomieszczeń roboczych stężenie par dwusiarczku węgla w powietrzu powinno wynosić do 1 mg/m3.
- Pochodne nitro- i aminowe oraz ich homologi reprezentują rozszerzoną grupę rozpuszczalników. Przewlekły obraz zatrucia wyraża się w postaci bólu głowy, apatii, niebieskawego zabarwienia skóry, zaburzeń czynności wątroby i ośrodkowego układu nerwowego.
W przypadku pomieszczeń roboczych stężenie par analitu w powietrzu nie powinno przekraczać 0,1 mg/m3, związków benzenu i toluenu – do 1 mg/m3.
Utylizacja odpadów
- Problem z recyklingiem jest istotny w działalności przemysłowej. Niektóre firmy zwracają się o pomoc do wyspecjalizowanych firm. Zniszczenie powinno być bezodpadowe i nieszkodliwe zarówno dla ludzi, jak i środowiska.
- Związki chemiczne i ich mieszaniny są toksyczne, aktywne, a wiele z nich jest palnych i wybuchowych. Opary wytwarzane przez te lotne substancje powodują nieodwracalne szkody dla ludzi i przyrody. Dlatego do procesu należy podchodzić z zachowaniem zasad bezpieczeństwa, w tym z użyciem środków ochrony indywidualnej.
Strona 1
Rozpuszczalniki węglowodorowe – pirokondensat, KOH-47-88 i zużyta nafta nie zawierają parafiny, żywic i innych naturalnych emulgatorów, dlatego nie tworzą emulsji z wodą lub z hamowanym kwasem solnym. Emulsja przygotowana z użyciem wymienionych rozpuszczalników i roztworu kwasu lub wody rozwarstwia się kilka minut po przygotowaniu. Jeśli roztwór zawiera 0 5% lub więcej emulgatora SKN-26, ta mieszanka w temperaturze 30 C nie płynie.
Rozpuszczalniki węglowodorowe są szeroko stosowane w przemyśle farb i lakierów ze względu na ich niski koszt i dostępność. Ta grupa rozpuszczalników obejmuje nasycone węglowodory serii alifatycznej (parafiny lub alkany) СlН2я 2, węglowodory alicykliczne o ogólnym składzie С Н2 i węglowodory aromatyczne .
Rozpuszczalnik węglowodorowy - pozostałość kadzi oleju - KOH - 47 - 88 to odpad poprodukcyjny przydomowych zakładów przemysłu chemicznego. Gęstość mieszaniny wynosi 850 - 900 kg/m3, lepkość kinematyczna w temperaturze 20 C wynosi 1 mPa - s, temperatura początku i końca wrzenia 88 - 180 C.
W tym przypadku rozpuszczalnik węglowodorowy praktycznie nie ma wpływu na pełzanie monokryształów cyny, będąc tym samym nieaktywnym ośrodkiem.
Rozpuszczalniki węglowodorowe są szeroko stosowane w wielu różnych gałęziach przemysłu. O ich zastosowaniu decyduje udana kombinacja wysokiej zdolności rozpuszczania węglowodorów w stosunku do szerokiej gamy związków organicznych o stosunkowo niskiej toksyczności i braku działania korozyjnego.
Rozpuszczalniki węglowodorowe mają średnią masę cząsteczkową.
Rozpuszczalniki węglowodorowe są bardziej miękkie niż rozważane; Nie usuwa barwników z materiałów tekstylnych i nie wypłukuje naturalnego tłuszczu z włókien wełnianych, zamszu i skóry. Rozpuszczają natomiast tłuszcze, wosk pszczeli, olej rybny, wydzieliny potu, oleje roślinne i smarne, smołę, wosk, parafinę, smołę, kalafonię, gumę, bitum i inne substancje. Rozpuszczalniki te nie niszczą takich włókien jak acegochlorin, polichlorek winylu, polichlorek winylu itp. Są mniej toksyczne i raczej tanie. Wadą rozpuszczalników węglowodorowych jest palność i zagrożenie wybuchem ich mieszanin z powietrzem.
Rozpuszczalniki węglowodorowe są klasyfikowane jako palne i wybuchowe substancje toksyczne. Większość z nich jest bardzo niestabilna. Pary rozpuszczalników są kilkakrotnie cięższe od powietrza, gromadzą się w niskich miejscach w słabo wentylowanych pomieszczeniach oraz w pobliżu maszyn, co może doprowadzić do wybuchu lub zatrucia.
// Rozpuszczalniki
Rozpuszczalniki to związki chemiczne zdolne do rozpuszczania różnych substancji, tj. do tworzenia z nimi jednorodnych mieszanin o zmiennym składzie z dwóch lub więcej składników.
Rozpuszczalnik jest jednym z najistotniejszych składników w produkcji substancji błonotwórczych. Najpopularniejszym rozpuszczalnikiem w przyrodzie jest zwykła woda, ale w przemyśle farb i lakierów rozpuszczalnik ten jest używany głównie do produkcji farb wodnych, podkładów i lakierów. Rozpuszczalniki organiczne są znacznie bardziej rozpowszechnione wśród rozpuszczalników do farb, emalii i lakierów. Wszystkie rozpuszczalniki organiczne stosowane w przemyśle farb i lakierów można podzielić na następujące sześć grup ze względu na charakter chemiczny:
1) węglowodory - alifatyczne, alicykliczne, aromatyczne, a także ropa naftowa i terpen;
2) ketony;
3) etery i estry;
4) alkohole;
5) rozpuszczalniki chlorowcowane;
6) inne rozpuszczalniki.
Rozpuszczalniki węglowodorowe są szeroko stosowane w przemyśle farb i lakierów ze względu na ich niski koszt i szeroką dostępność.
Do tej grupy rozpuszczalników należą nasycone węglowodory alifatyczne (parafiny lub alkany), węglowodory alicykliczne oraz węglowodory aromatyczne.
Rozpuszczalniki węglowodorowe otrzymywane są przez suchą destylację drewna i węgla, benzyny łupkowej, ropy naftowej i gazu naftowego.
Obecnie głównym naturalnym źródłem większości rozpuszczalników węglowodorowych jest olej.
Zawiera głównie węglowodory parafinowe, naftenowe i aromatyczne. W zależności od rodzaju oleju panuje w nim jedna lub inna klasa węglowodorów.
Ale frakcje olejowe destylowane w szerokim zakresie temperatur składają się z mieszaniny węglowodorów o różnych strukturach chemicznych.
Węglowodory alifatyczne – w przemyśle farb i lakierów stosuje się głównie parafiny.
Izoparafiny są szeroko stosowane za granicą, ponieważ są praktycznie bezwonne (zapach rozpuszczalników organicznych wynika z ich dużej lotności i należy do szkodliwych czynników pracy z rozpuszczalnikami). Izoparafiny są wykorzystywane do tworzenia powłok niskotoksycznych, w medycynie do produkcji chirurgicznych materiałów szewnych itp.
Węglowodory alicykliczne mają ograniczone zastosowanie w produkcji i technologii nakładania powłok malarskich i lakierniczych, chociaż mają większą zdolność rozpuszczania niż rozpuszczalniki alifatyczne i mniejszą toksyczność niż rozpuszczalniki aromatyczne. Głównym naturalnym źródłem tych rozpuszczalników jest olej.
Rozpuszczalniki alicykliczne są szeroko stosowane w produkcji włókien syntetycznych, rzeźbiarskich i farb drukarskich.
Największe zastosowanie jako rozpuszczalnik ma cykloheksan, który służy do rozpuszczania etylocelulozy, olejów i tłuszczów, wosków i gum.
Węglowodory aromatyczne to największa grupa rozpuszczalników węglowodorowych wytwarzanych przez przemysł chemiczny.
Obecnie węglowodory aromatyczne pozyskiwane są głównie z frakcji ropy naftowej metodami reformingu katalitycznego i pirolizy oraz w znacznie mniejszym stopniu z przeróbki węgla.
Przemysł krajowy produkuje prawie wszystkie rozpuszczalniki aromatyczne.
Rozpuszczalniki aromatyczne mają większą zdolność rozpuszczania niż inne rozpuszczalniki węglowodorowe i jako składniki składowe są zawarte w większości mieszanych rozpuszczalników.
Rozpuszczalniki aromatyczne obejmują benzen, toluen i ksylen, izopropylobenzen, rozpuszczalnik, tetralinę i dekalinę.
Aby scharakteryzować rozpuszczalniki naftowe, zjednoczone terminem „nefras” (rozpuszczalnik naftowy), stosuje się znaki charakteryzujące ich skład węglowodorów i frakcji; te ostatnie określają podstawowe właściwości fizykochemiczne rozpuszczalników.
Wskazane są również inne parametry, takie jak temperatura zapłonu.
W zależności od składu węglowodorów rozróżnia się następujące rodzaje rozpuszczalników naftowych:
Nefras-S - rozpuszczalniki o mieszanym składzie, w których występują węglowodory wszystkich grup (ale nie więcej niż 50% udziału masowego węglowodorów z każdej grupy).
Nefras-A - rozpuszczalniki z przewagą węglowodorów alifatycznych i obniżoną zawartością węglowodorów aromatycznych (nie więcej niż 2,5%).
Nefras-I - rozpuszczalniki izoparafinowe.
Nefras-P - parafina zawierająca ponad 50% udziału masowego węglowodorów parafinowych.
Nefras-N - z przewagą węglowodorów naftenowych.
Najważniejsze właściwości użytkowe rozpuszczalników naftowych to:
Zdolność do rozpuszczania związków organicznych;
Zdolność do usuwania zanieczyszczeń organicznych z powierzchni metali;
Zdolność do szybkiego parowania;
Zdolność do minimalizacji powstawania osadów jego składników;
Agresywność korozyjna (określona przez obecność związków siarki w rozpuszczalnikach);
Stabilność jakości rozpuszczalników naftowych, która charakteryzuje się ich gwarantowaną trwałością.
Przykładami rozpuszczalników naftowych są: benzyny, benzyna lakowa, rozpuszczalniki heksanowe i heptanowe.
Węglowodory terpenowe są jedną z dobrze znanych klas rozpuszczalników roślinnych.
Należą do nich naturalne i syntetyczne węglowodory.
Terpeny są zawarte w olejki eteryczne kwiaty, liście różnych roślin, w żywicach naturalnych (balsamy), w igłach i drewnie drzew iglastych (sosna, świerk, jodła, jałowiec, modrzew).
Powszechnie stosowane rozpuszczalniki terpenowe obejmują terpentynę, dipenten, olejek sosnowy (olejek sosnowy) i izopropyltoluen.
Ketony są rozpuszczalnikami większości substancji błonotwórczych.
Ketony alifatyczne i cykliczne są wykorzystywane w przemyśle farb i lakierów.
Spośród alifatycznych ketonów granicznych szeroko stosowane są: aceton, keton metylowo-etylowy, keton metylowo-izobutylowy, keton diizobutylowy i alkohol diacetonowy.
Główną zaletą ketonów alifatycznych jest ich wysoka zdolność rozpuszczania i stosunkowo niska toksyczność.
Spośród ketonów cyklicznych zastosowano cykloheksanon i metylocykloheksanon.
Są bardziej toksyczne niż ketony alifatyczne.
Etery obejmują pochodne alkoholi jednowodorotlenowych i dwuatomowych (glikoli) oraz ich związki cykliczne.
Spośród pochodnych jednowodorotlenowych alkoholi alifatycznych stosuje się etery dietylowe i dibutylowe.
Największym zainteresowaniem cieszą się monoalkilowe etery glikolu etylenowego – cellosolve i glikolu dietylenowego – karbitole.
Estry to najpowszechniejsza klasa rozpuszczalników organicznych o wielkich praktycznych zastosowaniach.
Estry wytwarza się przez estryfikację odpowiednich alkoholi kwasami mineralnymi lub organicznymi.
h Jako rozpuszczalniki najszerzej stosowane są estry kwasu octowego, octany (octan metylu, octan etylu, octan butylu).
Inne estry (kwasy mlekowe – mleczany, masłowy – maślany, mrówkowy – mrówczany) znalazły ograniczone zastosowanie, m.in. ze względu na dość wysoki koszt.
Ze względu na ich silne zmydlanie i wysoką toksyczność, mrówczany prawie nigdy nie są obecnie stosowane.
Alkohole są również szeroko stosowane jako rozpuszczalniki.
Najczęściej spotykane to metanol, glikol etylenowy, gliceryna, pentaerytrytol, butanol, izopropanol.
Wśród rozpuszczalników najbardziej rozpowszechnione są różne klasy alkohole: jedno- i wielowodorotlenowe; alifatyczne i cykliczne.
Alkohole są rozpuszczalnikami polarnymi i są stosowane w wielu różnych gałęziach przemysłu.
Najpopularniejszym alkoholem wśród rozpuszczalników jest etanol – jego światowe zużycie w tej pojemności wynosi nieco mniej niż 4 mln ton rocznie.
Inne popularne rozpuszczalniki to metanol i izopropanol, których zużycie wynosi ponad 1 mln ton rocznie.
Zastosowanie alkoholi jako rozpuszczalników obejmuje następujące obszary: rozpuszczalnik procesowy, rozpuszczalnik do produkcji farb i powłok, zmywacz, rozpuszczalnik do produkcji wyrobów konsumpcyjnych, rozpuszczalnik aerozolowy.
Rozpuszczalniki chlorowcowane (chlorometany, chloroetany, rozpuszczalniki zawierające fluorochlor, wodorofluoroalkany) mają najwyższą zdolność rozpuszczania, a na ich podstawie otrzymuje się wysokiej jakości środki odtłuszczające.
Takie rozpuszczalniki stosuje się w szczególności do odtłuszczania butli tlenowych lub manometrów.
Rozpuszczalniki te charakteryzują się zmniejszoną palnością, mają lepszą lotność niż większość rozpuszczalników i są bardziej efektywne.
Ich główną wadą jest bardzo wysoka toksyczność.
Ich zastosowanie w znacznym stopniu przyczynia się do efektu cieplarnianego i „kwaśnych” deszczy iz tego powodu zaliczane są do materiałów prowadzących do zniszczenia warstwy ozonowej ziemskiej atmosfery. Z tego powodu są oczywiście bardzo nielubiane przez ekologów.
Rozpuszczalniki muszą być chemicznie obojętne w stosunku do substancji rozpuszczonej, tj. nie powinien wchodzić z nim w interakcje chemiczne.
Rozpuszczalniki powinny mieć niską higroskopijność: nawet przy niewielkiej ilości wody ich zdolność rozpuszczania gwałtownie spada.
Rozpuszczalniki organiczne są toksyczne, one (i ich opary) mają szkodliwy wpływ na ludzi.
Podczas pracy z nimi należy bezwzględnie przestrzegać środków bezpieczeństwa, w szczególności zapewnić dobrą wentylację pomieszczeń i, jeśli to konieczne, używać sprzętu ochronnego - rękawic i respiratorów.
Podczas pracy z rozpuszczalnikami należy wziąć pod uwagę ich zagrożenie pożarowe.
Zdecydowana większość rozpuszczalników organicznych jest palna, a mieszanina ich oparów z powietrzem w określonym stężeniu tworzy mieszaninę wybuchową.
Dlatego w pomieszczeniach, w których przechowywane są rozpuszczalniki i wykonywane są z nimi prace, należy ściśle przestrzegać zasad bezpieczeństwa przeciwpożarowego.
