Фенолфтене гэж юу вэ. Усны ууртай нэрэх үед үндсэн аюул.
(Баримт бичиг)
n2.doc.
Боловсролын байгууллага боловсролын байгууллага
Ерөнхий туршилт 1: Титролт
Сүүлийн хэдэн дусал ус нэмэх үед яагаад нүд чинь толботой байх ёстой вэ?
- Энэхүү стандарт шийдлийн концентраци юу вэ?
- Шилэн, юүлүүрийг усаар угаах зорилго нь юу вэ?
- Хэмжилтийн колбыг усаар услах зорилго нь юу вэ?
Халуун архины аргыг дахин боловсруулах арга
Ширээнээс, энэ туршилтын дундаж дүнг тодорхойлж, энэ утгыг өөрийн тооцооллын үлдэгдэлд ашиглана уу. Өмнөх жишээг ашиглан цууны цууны агууламжийн агууламжийг тодорхойл. Дараахь мэдээлэл байгаа эсэхийг санаарай: натрийн гидроксидын уусмалын хэмжээ, натрийн гидроксидын шийдэл. Үл мэдэгдэх концентраци бүхий натрийн гидроксидын шийдлийг тодорхойлох.
Улс гурэн боловсролын байгууллага Мэргэжлийн өндөр боловсрол
Парссибаатар төгс сургууль M. V. Ломоносов
Химийн тэнхим
Хичээлийн ажил
Синтезийн фенолфтейлин.
Өөр өөр Dielectrical Confaction ашиглан уусгагч уусгагчдыг судалгаа хийх
Гүйцэтгэсэн:
Төвлөрсөн хүчил ба суурь нь ноцтой түлэгдэх шалтгаан болдог. Та хүчил эсвэл суурьтай ажиллахдаа бээлий, аюулгүй шил ашиглахыг санал болгож байна. Бурет хаалттай байгаа эсэхийг шалгаад oxettal-ийн стандарт шийдлийг булшлах хүртэл зөөлөн шийднэ. Шилэн шилийг хүнд суртлын дагуу байрлуулж, оксалик хүчилд үүний уусгагчийн уусгагчийн хэсгийг сайтар байрлуул. Энэ нь АВТОМАШИНГИЙН АМЬДРАЛЫН АГААР АВТОМАШИНГИЙН ТӨЛӨВЛӨГӨӨГҮЙ БАЙНА. Шийдлийн дээд хэсэг нь 0 ба 1 см-ийн хоорондох тэмдгийн хоорондох байх ёстой. Конусын колбонд 20 см 3-ийн уусмалыг хэмжих пипеткийг ашиглана уу. 3-4 дусал Фенолфтеинийг конус хэлбэртэй колбонд нэмнэ. Конталь колбонд оксалик хүчил нэмээд, контик колбонд хурдан ээрэх Уусмалын өнгө өөрчлөгдөх тусам дахин зогсоож, тохой өөрчлөгдөнө. Хэрэв колбо ээрэх үед өнгө өөрчлөгдөхгүй бол өнгө нь өнгө үлдэх хүртэл илүү оксалик хүчил нэмнэ. Хоёрдахь конус колбо 4-7 алхамыг давт. Та 2 см 3 см-ийн титрийн хэмжээнээс 2 см 3-аас бага хэмжээгээр ockaly колбонд оксиалийн хүчил нэмнэ. Дээр энэ мөч Өнгө нь урт хугацааны өөрчлөлт байх ёсгүй. Аажмаар оксалик хүчил нэмнэ. Дусал бүрийн хооронд эргэлдээд шаардлагатай бол колбоны хажуу талыг усаар зайлна. Уусмал нь өнгийг өөрчлөхөд шинээр өөрчлөгдөж, шинэ хэвээр байна. Гарчигны хэмжээ: -. Нарийвчлалтай, 9-11-р алхамуудыг давтана, 9-11, 1-ээс хэтрэхгүй байх ёстой.
- Нүдний шилний нэгийг тэмдэглээрэй \\\\.
- 100 см 3 см-ийг шилэн хэмжихийн тулд Pipette ашиглана уу.
- Ойролцоогоор 4 гр-ийг шилэн рүү шилжүүлээд холино.
- Бага зэрэг товчийг дарж, Дээрхээс жижигхэн юүлүүр байрлуул.
- Фенольфтенеенийг нэмж байхад натрийн гидроксидын уусмал байсан уу?
- Хүчилт нь хангалттай хэмжээний нэмж байхад ямар өнгө байсан бэ?
оюутны 3 курс
химийн хэлтэсүүд
Vladimir Ivanovich leferes
ТУХог Шалгасан:
Appleiate профессор, л. Хоёр. Шинжлэх ухаан
Ovandowskaya t. V.
Appleiate профессор, л. чи яаж Шинжлэх ухаан
Chagin n. B.
Аркангонс
1. Уран зохиолын тойм ................................................ ........ ..5
Фенольфтейлийн гадаад төрх ба физик шинж чанар ............ .5
Фенольфефеиныг ашиглах .........................................................
Химийн шинж чанарууд .................................................................. ... ... 8
Фенольфефейлин авах .................................................................
1.4.2 Биеийн хөгжлийн шинж чанарууд Синтезид ашигладаг бодисууд ... .15
Өмнөх жишээг ашиглан натрийн гидроксидын шийдлийн концентрацийг тодорхойл. Танд дараахь мэдээлэл байгаа бол: Covey Hydroxide-ийн арилжаагаар оксейн хүчиллэг шийдлийн тунгалаг арилжа. Энэ урвалын тэнцвэртэй химийн тэгшитгэл.
Оюутны хүчлийн массыг тооцоолох нь шаардлагатай стандарт шийдлийг хөрвүүлэхийн тулд уусдаг. Энэ нь хямдралтай хүчиллэгийн тусламжтайгаар 40 см 3-ийг үзэж байна. 35 см-ийн 3 см-ийн гидроксиденийг саармагжуулж байна.
- Бидэнд оксейн хүчил хэрэгтэй.
- Гэсэн хэдий ч бид мольтын тоог хараахан мэдээгүй байна.
1.4.3 Усны ууртай нэрэх аргууд .................................... 16
1.4.4 Халуун архи, халуухан архины арга ............ .18
1.5 Аюулгүй байдал .............................................. ... 20
1.5.1 Төвлөрсөн хүчилтэй ажиллахдаа үндсэн аюул ................................... .......................................... ......... 20 20
Усны ууртай нэрэх явцад 1.5.2 ХӨДӨЛГӨӨН Аюул :... ..21
- Урвалын тэнцвэртэй химийн тэгшитгэлийг бичнэ үү.
- Хүчиллэг агууламжийг тооцоолох.
Энэ бороо ихэвчлэн хүчиллэгийг анх удаа тэмдэглэжээ, гэхдээ хорьдугаар зууны үед энэ хүчиллэг нь "хүчиллэг" нь хүчиллэг "нь" хүчиллэг "нь" хүчиллэг "нь" хүчиллэг "нь" хүчиллэг "нь" хүчиллэг "-ийг" хүчиллэг "-д ачдаг бөгөөд энэ нь хүчиллэг" нь хүчиллэг "нь" хүчиллэг "-т" хүчиллэг "-ийг" хүчиллэг "гэсэн үг юм. Гол кулпит нь нүүрс нь хүхэрийг бохирдуулж байсан нүүрс. Цахилгаан станц дээр шатаж байх үед энэ сульфур нь хүхөрөгчийн давхарга, уур амьсгалтай, уур амьсгалыг дамжуулж өгдөг.
1.5.3 Халуун архи, согтууруулах ундаа хэтрүүлэн бодоход үндсэн аюул ...................................... .......................................... .......................................... .......................................... ..
1.5.4 Синтезид ашигладаг бодисуудтай ажиллах функцүүд ................................................. .......................................... 22
1.6 Шүршүүрийн шинж чанар .................................... 24
1.6.1 Бие махбодийн шинж чанараараа уусгагчийн ангилал ... 25
Хүхрийн хүчил нь маш хүчтэй хүчил, мөн ус борооны дусал, усанд хүчил уусна үүсэх агаараас хамтад үед. Дараа нь бороо унаж, цэвэр усны биед угсарч, хүчиллэгийг нэмэгдүүлдэг. Хойд Зүүн Америкийн Нэгдсэн Улс, энэ нь хамгийн их зовсон, учир нь Ohio хөндийд, Огайо болон Пенсильвани зэрэг сүүлийн нэг бүтэн, нэг хагас зууны нүүрсний салбарын ихэнх нь газар юм. Цаг агаарын давамгайлсан байдлаас шалтгаалан эдгээр утааны хий нь Огайо Хөндий уур амьсгалд ордог, гэхдээ бороо нь Нью-Йорк, Шинэ Английн хойд хэсэгт хүрч байна.
1.6.2 Системийн уусгагчийг үндэслэн суурилуулсан химийн шинж чанарууд………………………………………………..30
Хатуу уусах тодорхойлох 1.7 Тойм арга ......................................... ..................................................................................
1.7.1.1 Gravimetric арга ................................................................ .35
1.7.2 Электрочимын аргыг .............................................................................................................. 37
1.7.3.3.3 фотоэлектро-калориеметрийн арга ......................41 ..41
Борооны хүчиллэг өсөлт нь сүйрэлд хүргэж болзошгүй юм. Хөрсөнд ихэвчлэн бусад нэгдлүүдтэй нягт холбогддог хөрсөнд байдаг. Нэгэн цагт, Шинэ Английн олон цөөрөм нь үүнээс болж урсгалын форелийг хадгалах чадваргүй байсан. Ургамал нь бас хөрсний хамгийн мэдрэмтгий байдаг. Хэрэгтэй тэжээллэг бодисыг хөрсөөс нь усаар угааж, ургамлыг үл тоомсорлож чадахгүй. Ялангуяа хүчтэй нөлөөлсөн газар нутагт хэдэн арван үхсэн модыг хайж олох боломжтой.
2. Туршилтын хэсэг .............................................. .. 43
фенолфталейн 2.1 синтез .............................................. .. ... 43
2.2 Халуун архи, согтууруулах ундаа хэтрүүлэн бодох ..............................45
2.3 уусмалын тодорхойлолт ............................................................................ .47
Дүгнэлт ........................................................... .................... 50. 50.
Ном зүйийн жагсаалт .......................................................... .51
Барилга, хөшөөг нь чулуу иддэг хүчил бороо, ялангуяа шохойн чулуу иддэг. Баримал, булшны чулуулаг, булшны чулуунууд, бүр зарим барилгууд асар их алдагдалд хүргэсэн - зарим урлагийн бүтээлийг бүрэн устгасан.
Тэр авууд гарин нь гаралшалт нь ихээхэн буурч, хүчиллэг бороо мөн буурчээ. Гэсэн хэдий ч асуудал хараахан дуусаагүй байгаа бөгөөд энэ нь байгаль орчны ноцтой асуудалд үүнийг арилгаж чадахгүй байна. -ийн давсны хүчил, ихэвчлэн "шүлтийн" гэж нэрлэх нь бий ходоод хүчил, натрийн гидроксид, гол бүрэлдэхүүн хэсэг юм, саван хэрэглэж байна авч үзье. Гэсэн хэдий ч бараг бүх гидронон, гидроксид нь ус молекулыг услах, натрийн хлорид, натри ионуудыг орхиход нэгтгэдэг.
Оршил
Фенольфтейлин бол хүчиллэг үндсэн үзүүлэлтүүдийн химийн агуулгад хамгийн өргөн хэрэглэгддэг. Энэ нь Triarilmetan-ийн будаг, Phthalein гэж нэрлэгддэг.
Энэ ажлын зорилго нь Фенольфелийн синтезеин бөгөөд өөр өөр Dielectrire-ийн синтентийн синтезийг судалж үздэг. Энэ зорилгодоо хүрэхийн тулд дараахь даалгавруудыг шийдэх ёстой.
Хэрэв дийлэлтийн хүчилдэт хэмжээ нь натрийн гидроксид яг ижил хэмжээтэй байвал гидрони нь одоо төвийг сахисан байдаг. Одоо энэ нь 7 болон үүнтэй нэг шил цэвэр ус байх ёстой. Бид маш их идэмхий бодисоор эхэлж, үр дүнтэй бүтээгдэхүүнээр төгсдөг.
Ерөнхийдөө хүчил, суурь нь бие биентэйгээ харьцахад бие биенээ саармагж, бие биенээсээ саармагж, уусмалын рН нь ойртоход хүргэдэг. Үүнийг "" гэж нэрлэдэг. Зөвхөн дараа нь тэнцүү хэмжээний хүчтэй хүчил, хүчтэй баазтай байх үед PH нь үнэн зөв байх болно. Гэхдээ олон тохиолдолд, сул хүчил ба сул баазыг хослуулсан. Гэсэн хэдий ч рН-ийг 7 ойртуулж, гэхдээ шийдэл нь төвийг сахисан биш байх болно. Хүчиллэг бороо, чулуу, хөрс, хөрс нь ихэвчлэн гол, ялангуяа карбонат чулуулагууд байдаг.
1. Энэ асуудлын талаар уран зохиолыг дүн шинжилгээ хийх;
2. Synthesis-ийн техникийг сонгоод тэдгээрийн хамгийн их хүлээн зөвшөөрөгдсөнийг сонгоно уу;
3. Бүтээгдэхүүнийг хуваарилах, хуваарилах, хуваарилах, цэвэрлэх;
4. Өөр өөр Dielectric-тай холбоотой уусмалыг өөр өөр Dielectric хийх замаар шалгаж, уран зохиолын өгөгдлийг харьцуулах үр дүнг харьцуул.
Хүчиллэг борооны сул хүчиллэг хүчлүүд чулуун дээр унадаг тул шавар, чулуун дээр навчис, чулуун дээр саармагжуулдаг. Гэсэн хэдий ч эдгээр үндэслэлүүд, жишээ нь, жишээ нь, чулуулагт сэргээгдэхгүй. Нэг зууны хүчиллэг бороо орсны дараа чулуунууд нь бүхэл баазыг саармагж, хүчиллэг бороог экосистемд оруулдаг бөгөөд үүнийг сахисан байдлаар саармагжуулдаг бөгөөд үүнийг саармагжуулдаг.
Фенолфтейлин: Ерөнхий лабораторийн үзүүлэлт
Фенолфтеин молекул нь суурь, ягаан, ягаан өнгөөр \u200b\u200bялгадас байдаг. Энэ бол энгийн хүчиллэгийн хүчиллэг титрацийн хүчиллэг титраци хийх гайхалтай үзүүлэлт юм. Титректын 5-р хэсэгт 8-р хэсэгт, хоёр шийдлийг хамтдаа хоёр шийдлийг хослуулсан арга нь хяналттай StoIchiomettric урвалын хариу үйлдэл хийх арга. Энэ нь мэдэгдэж буй концентрацийн уусмалыг шаарддаг бөгөөд ихэвчлэн үл мэдэгдэх концентрацид шилжсэн байдаг. Титраци хийхэд ямар нэгэн хариу үйлдэл хийх болно, гэхдээ хариу үйлдэл хийх үед хэлэх боломжтой байхын тулд хэлэх боломжтой байх ёстой, харагдах цэг байх ёстой.
5.
Хийсэн ажлын талаар дүгнэлт гаргах.
1. Уран зохиолын тойм
1.1 Фенольфтелийн гадаад төрх, физик шинж чанарууд
Фенолфталейн (ди-N-dioxidifenylphthaleide, 2,2 бис (N-hydroxyphenyl) phthalide) - цагаан, эсвэл бага зэрэг шаравтар талст нунтаг; ReCrystallization, өнгөгүй, ромын зүү нь этилийн архины улмаас үүсдэг. Фенольфтейлейн үнэрт тэсвэртэй биш, агаарт тэсвэртэй биш. Молекул жин нь 318.3 г / моль. Фенолфтейлин 250 ° C (258 08) ба түүнээс дээш хугацаанд хайлдаг Өндөр тоог Ажиллуулах.
Фенолфтейлин жингээ хасах хэрэгсэл шиг
Хүчиллэгээр нөлөөлсөн урвалын хувьд шалгуур үзүүлэлтүүд нь энэ төрлийн мэдээллийг өнгөний өөрчлөлттэйгээр тодруулах боломжтой. Тиймээс, хүчиллэг баазын саармагжүүлэх урвал нь тибризийн шинжилгээнд хэрэглэгддэг хамгийн түгээмэл төрлийн урвал юм. Тиймээс титрлийг үл мэдэгдэх шийдэлд байгаа хүчил эсвэл суурийн хэмжээг тодорхойлоход ашиглаж болно.
Хүчтэй баазтай хүчтэй хүчил титрэх үед Докт нь яг 7 нь 7-тэй байх үед эцсийн цэг нь зөвхөн төвийг сахисан электролиттай байх ёстой. Хүчил алга болохын дараа бид колбонд нэмж оруулахгүй аливаа суурь нь саармагжуулагчийг саармагжуулж, уусмалыг нэмэгдүүлэх болно. Гэхдээ хэт их суурь нь бюретк нь дусал бага ч гэсэн хувь нь рН-ийн нэг буюу ийм үзүүлэлт, phenolphthalene нь өөрчлөлтөд хүргэнэ, ил тод бөгөөд хүчиллэг уусмалд blundered, гэхдээ гол шийдэл нь энэ бол харанхуй ягаан болдог рН 2-оос дээш.
Сптольфтеинеин уусмал уусдаг уусмал уусмал уусдаг уусмал, хлороформ, хлороформ, ацетон, ацетон, тосолсон эфир, бензол, Тэсвен, Тэсвен, ХОЛТ, ТОГИУЛ, ХОЛБОО, ХОЛБОО, ХОЛБОО, ХОЛБОО, ХОЛБОО, ХУВЬЦАА, ХУВЬЦАА.
1.2 Фенольфтейлины хэрэглээ
Фенольфтейлин бол хамгийн өргөн хэрэглэгддэг импортын нэг бөгөөд ялангуяа сул хүчиллэг тодорхойлолтын нэг юм.
Энэ нь хэд хэдэн ашиг тустай: өндөр температурт мэдрэмтгий биш харин уураг, уураг, коллоидын оршихуйд алдаа гардаг. Архи согтууруулах ундаа агуулсан уусмалд ч гэсэн өргөн хэрэглэгдэж, шүлтлэгийн шийдлийн өнгө нь зөвхөн Alkali-ийн уусмалын өнгөт уусмалын өнгөний онцлог шинж чанараас ялгаатай. Төвлөрсөн согтууруулах ундааны шийдэлд, гол хэлбэр нь цэнхэр ягаан өнгөтэй байдаг. Фенолфтейлиныг архины уусмал, архи, эсийн хүчиллэг хүчиллэгийн гарал үүслийг тодорхойлоход ашиглаж болно. Хажорор ба Хиам нь Фенольфефенейн оршихуйд баазын цогцолборыг бий болгохыг санал болгож байна. Сэтгэл ханамжтай үр дүнг 2 · 10 -6 - 30 - 30 · 10 -6 · 10 -6 гротетр нь Фенольфтейлины дэргэд 10 -6 грот. Микагийн судалгааны дагуу Миккийн судалгааны дагуу микрокидиметрийн маш чухал үүрэг гүйцэтгэдэг. Фенолфтейлин бол олон холимог үзүүлэлтүүдийн нэг хэсэг юм. түүний чанар улмаас, энэ нь шийдэл буфер, эсвэл буфер уусмалын ямар Michaelis аргаар ашиглан рН калориметрийн тодорхойлоход тохиромжтой. Будсан хэлбэр нь BEARE хуулийг өргөн хүрээнд дагаж мөрддөг.
Олон төрөлд багтсан хүчиллэг үзүүлэлтүүд
Фенолфтенаалин 0-ээс бага зэрэг өөрчлөгдөж, дүрмийн дагуу бага зэрэг өөрчлөгдөж, туршилтанд маш бага алдаа гаргадаг. Фенолфтенаас гадна бусад үзүүлэлтүүд, бусад үзүүлэлтүүд нь Бромотимол цэнхэр, метил улбар шар өнгө орно. Зөвхөн төгсгөлийн цэгээс бага зэрэг ялгаатай, бромимал цэнхэр бол сайн үзүүлэлт юм. Докторын 7-ийн доор PH-ийн доор, шийдэл нь PH-ээс бага зэрэг цэнхэр өнгөтэй шар өнгөтэй шар өнгөтэй. Титриний эцсийн цэг нь илүү исгэлэн, метил улбар шар хэрэглэгддэг.
Фенолфтейлиныг өндөр чанарын шинжилгээнд уралдаан болгон ашиглаж болно. Саксагийн хэлснээр, Кадмайр, цайр, цайр, цайр, магни, Магниум, zinlphalene, zinolphalene-тай шүрших, заагчийг adsorpation. Өөр нэг бүлэг урвал нь шүлтлэгийн орчинд үндэслэн шүлтлэг орчинд суурилдаг, фенолфтейлин нь өнгөгүй фэнолфтенийг сэргээдэг. Энэхүү Leuke-ийн хяналт нь зарим бодисоор исэлддэг бөгөөд дараа нь Фенольфтфелийн улаан өнгө дахин гарч ирнэ. Зэсийн сульфатын ул мөр нь цианид ион (0.01-0.0.0.05 мг / L) ажиглагддаг. , Устөрөгчийн хэт исэл систем илэрцүүд болгон нэвтрүүлэх хяналт leuke исэлдлийн үйл явцын хурд нь нэмэгдэхэд - зэсийн маш бага хэмжээний (10 -5% 10 -4) нь.
phenolphthalene нь деривативын нэг phenolphthalaine фосфатын юм - фосфатазын ферментийн үйл ажиллагааг тодорхойлоход хэрэглэгддэг. phenolphthalaine фосфатын өөрөө үзүүлэлтийн шинж биш, харин ферментийн үйл ажиллагааг устгах; Фосфатын бүлгүүд нь субстратын нөлөөн дор хутгалдаж, фенолффелийн улаан зураг гарч ирнэ.
Анагаах ухаанд, Фенолфтенаалин нь LAXALION-д ашиглагддаг бөгөөд мансууруулах бодис хэрэглэдэг, эмийг дууддаг.
1.3 Химийн шинж чанар
Фенолфтефийн зураг төслийн хөндлөн огтлол нь 8.2 (өнгөгүй) -ийг PH 9.8 (нил ягаан) хооронд хэлбэлздэг. Шилжилтийн интервал, цуврал буферийн шийдлийг тодорхойлохын тулд: 7.8-8.2.8.4-8.6-9.6-9.0-9-9-9-9.8-9-9-9-10.0-10.0-10.0-10.2.2. Эхний сарнайн толбо нь илэрдэг PH утгыг илтгэнэ, үзүүлэлтийн концентрациас хамаарна. Нил ягаан өнгийн өнгөний эрчмийг аажмаар рН-ийг аажмаар сайжруулдаг. PH 1/2 9,53.
quinoid бүтэц (III) нь хэрчсэн уусмал (pH8,5) шингэлж нь хамт фенолфталейн харилцан үйлчлэлийн үр дүнд үүсдэг өнгөтэй diagnon бүрдүүлэх үйл явц нь дараах байдлаар илэрхийлж болно:
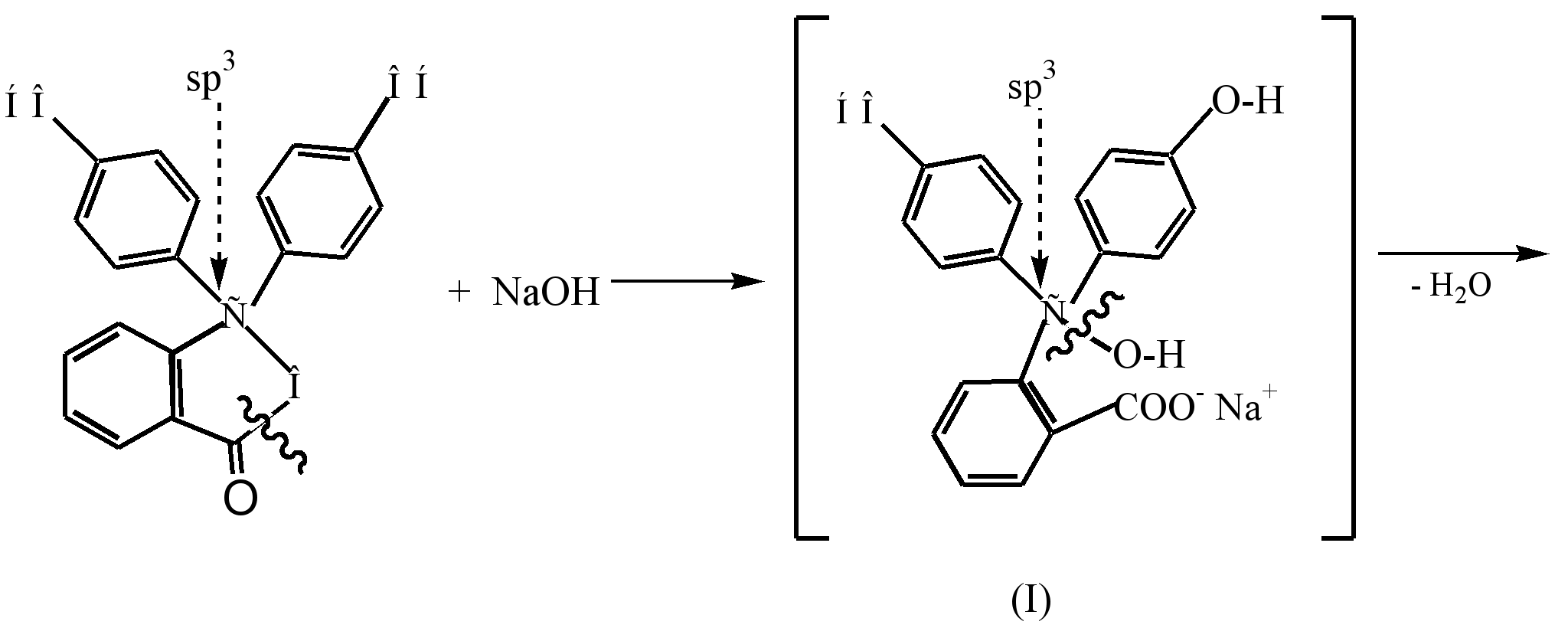

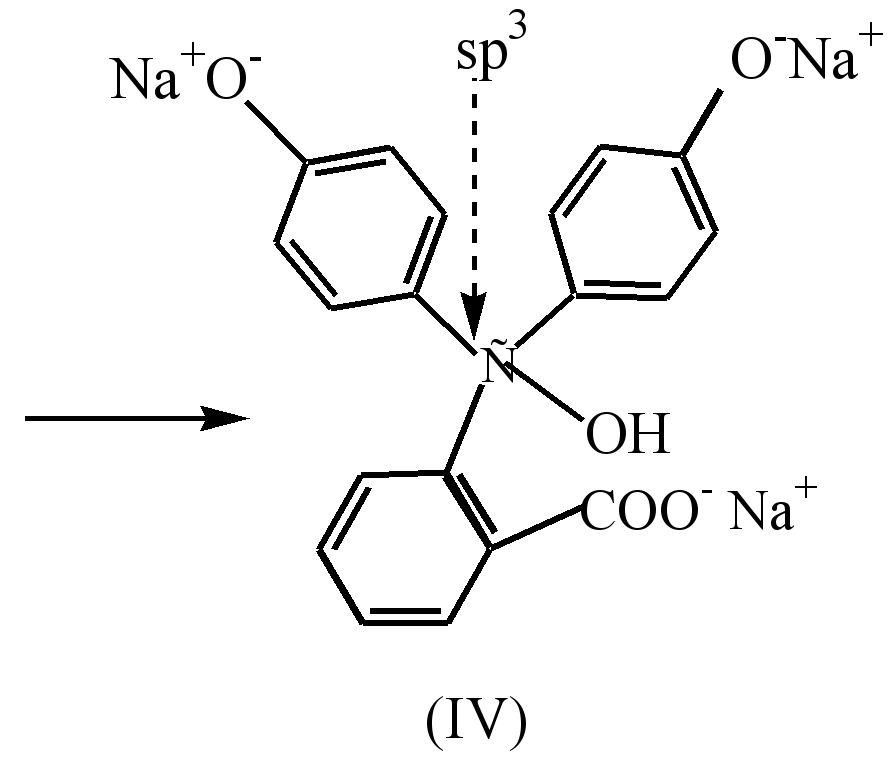
Өнгөгүй фэнолфтенений хийсэн үйлдлийн дор нээлтийн дор (гидролиз)? Offtric Rep (i) нь усны молекулыг (i) шар өнгийн молекул (II) -ийг аяндаа (i) шар өнгийн молекулыг бүрдүүлдэг. нь ditrium давс (III) үүсэх ба Бөөрөлзгөнө, conjugation гинжин уртсалт улмаас юм гүнзгийрүүлэх өнгө нь давирхай илэрцүүд цаашид харилцан.
нь strongshop дунд (pH10) байдаг trinitric давс (IV) нь цагираг коньюгат биш юм руу Натрийн давс (III) шилжилтийн үр дүнд уусмалын өнгө юм.
Хүчиллэг орчинд, сул дорой бензой хромофор тусгаарлагдсан, бие даан, бие даасан, үү? - харилцан үйлчлэл (хослуулах) бие биетэйгээ нэвтрэхгүй:
Тэд SP SP 3 - Нүүрстөрөгчийн атомыг дамжуулагч, дамжуулагч биш харин тусгаарлагч юм. - электронууд. , Тохиргоо нь удирдаач болох - SP 2 атом авсан - нь шүлтлэг орчинд, фенолын hydroxyls нэг ionizes болон SP 3, lactone мөчлөг эвдэрсэн байна вэ? - Бензой хромофорын хоорондох электронууд, ижил туйлширсан AUXOCHROMAS-ийн хоорондох электронууд - SOO - ба -O. Төвлөрсөн хүдэрийн хүчилтүйц, үзүүлэлтийг улбар шар өнгөөр \u200b\u200bбудаж байна. Өнгөт карбоксилийн бааз үүсэх үед нүүрний ягаан өнгийн шөрмөсний шилжилтийн эрч хүч (энэ нь эргэлт буцалтгүй агаарын исэлдэлт)
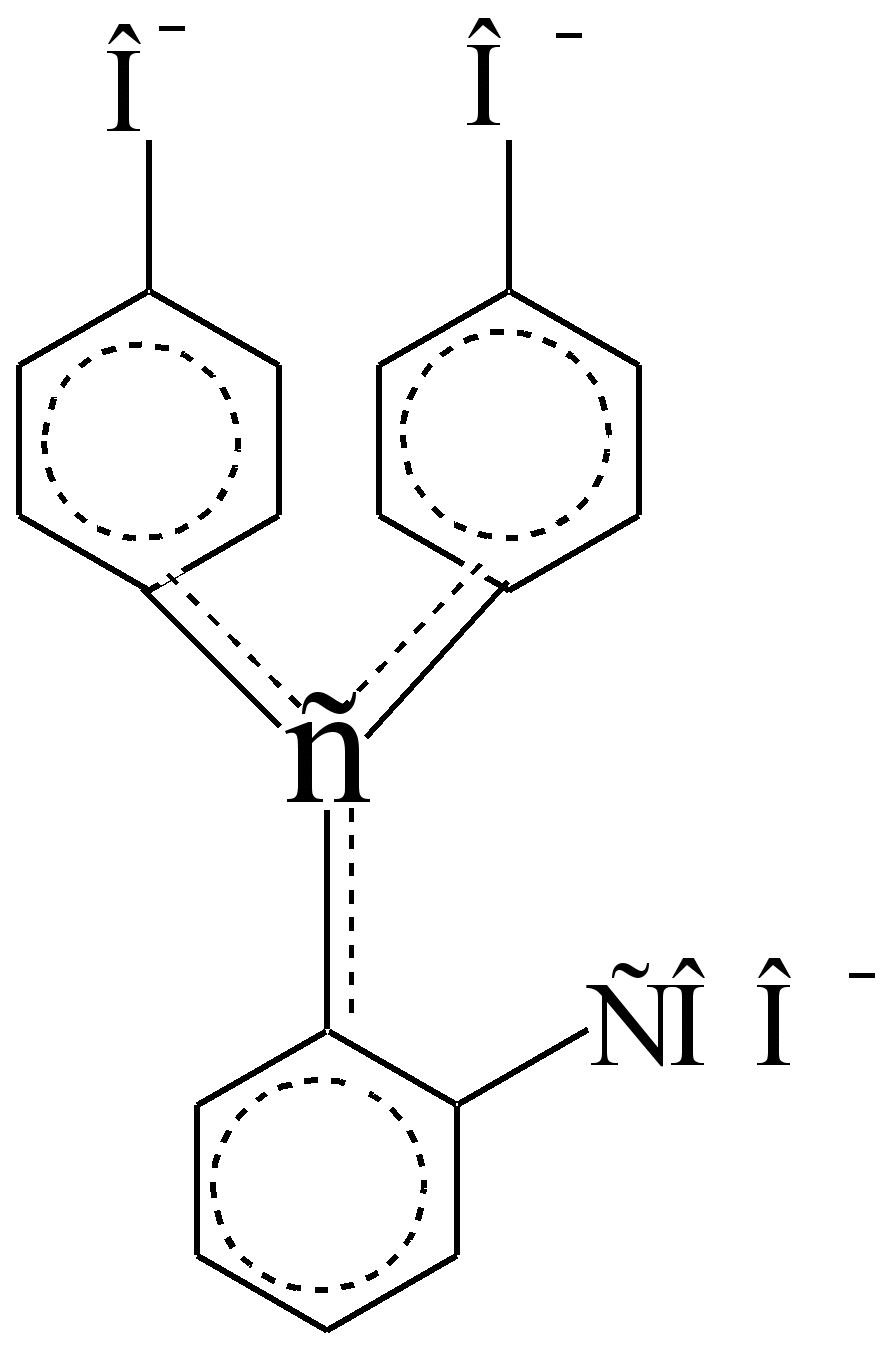
Фенолфтейн хромофтеле
(Шүлтлэг хэлбэр, 1 \u003d 553 NM, 1 \u003d 9000)
1.4 Фенольфтейлейн бэлтгэл
Фенольфтейлейн олж авах гол арга бол фенолик антидридын фенозын конденсац юм. Энэ урвал нь Friedel-Kraft-ийн дагуу акулын онцгой тохиолдол юм. Хүчиллэг катализаторын тусламжтайгаар урвал үүссэн тохиолдолд урвал үүсдэг (төвлөрсөн сульфурын хүчил эсвэл цайр хлорид):
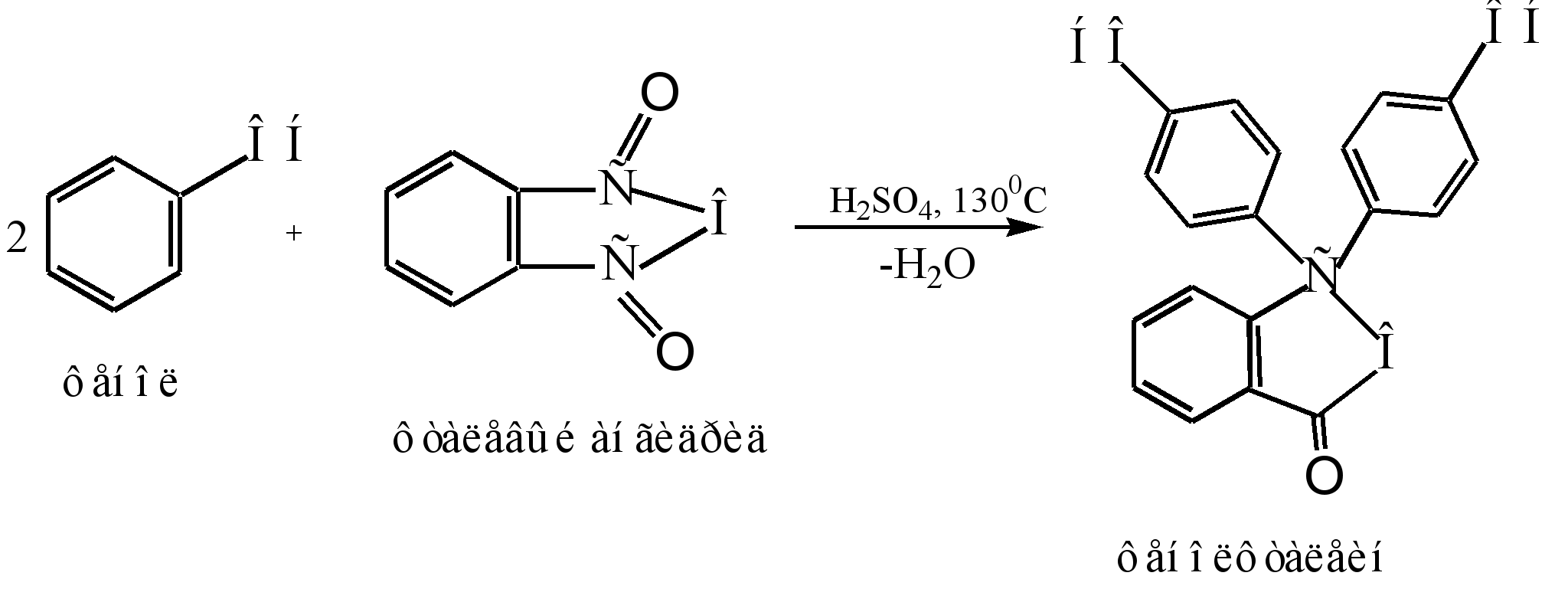
Урвалын механизмыг дараах байдлаар төлөөлж болно.

Sigma - нарийн төвөгтэй
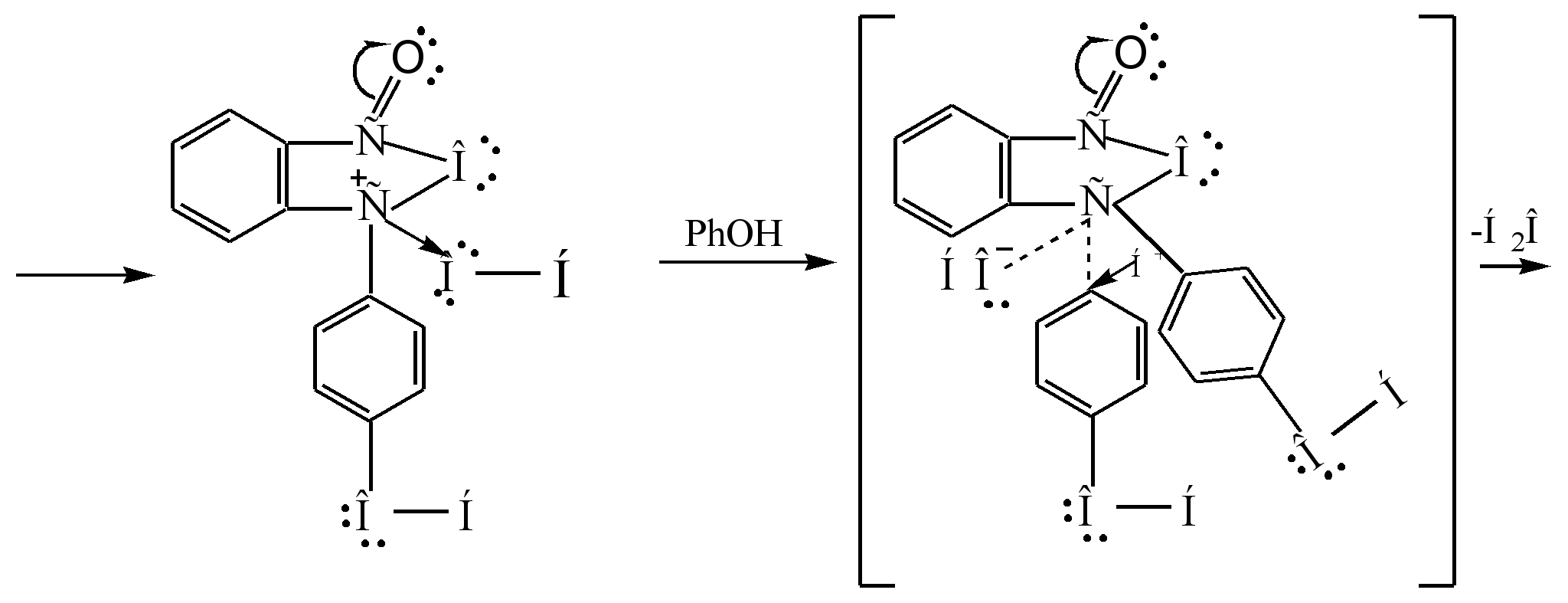
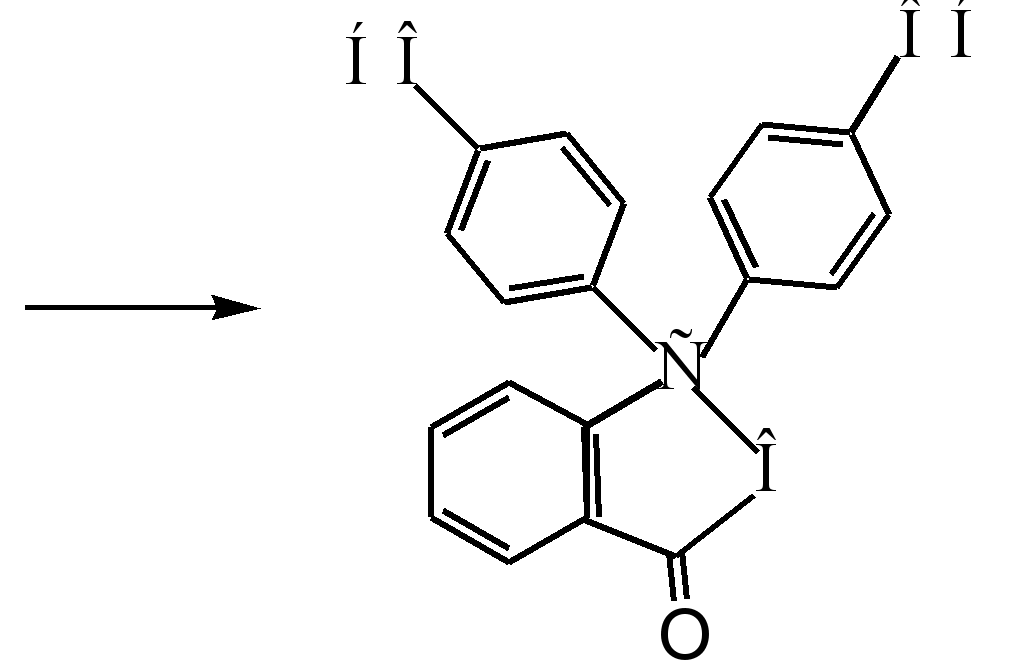
фенолфтейлин
1.4.1 Фенольфтена мужийн үйлдвэрлэлийн техник
Энэ талаар уран зохиолын эх үүсвэрийг шинжлэх дараа бүх арга ашиг, фенолфталейн олж авах нэг арга өгсөн байна гэдгийг олж мэдсэн байна. Энэ нь дээр дурдсан хариу үйлдэл дээр үндэслэсэн болно. Техник нь манай лабораторийн нөхцөлд бүрэн тохиромжтой.
Синтезийн хувьд дараах урвалжууд, аяга таваг, аяга, тоног төхөөрөмж шаардлагатай болно.
Phthalic Anhydride-5G; фенол-10г; хүхрийн хүчил - 2 мл; натрийн гидроксид - 4-5%; цууны хүчил (төвлөрсөн); гидрохлорик хүчил (төвлөрсөн); Этилийн архи (үнэмлэхүй).
Колбоны дугуй хүрээ (50мл) - 1 PC; Шил (100мл) - 1 PC .; Шаазан шаазан аяга - 1 PC .; конусын колбо (250ml) - 2 PCS .; термометр; Усны ууртай нэрэх төхөөрөмж; Ванны элсэрхэг.
Синтези шилжих:
5G Phelecile Anhydride, 10G фэнол, 2 мл-ийн хүчилтөрөгчийг 1,5 цаг, температурт байрлуулж, агшин зуурын усанд оруулав. Байна уу. Халуун хольцыг 100 мл буцалж буй ус руу залгаж, феноол урвалд ороогүй усны уурын тусламжтайгаар 100 мл буцалж буй ус руу залгав. Тасралтгүй, холбоотой бодисын алдагдал, шингэний алдагдал, шингэнийг үргэлж холих ёстой. Дадлага хийх төгсгөл нь чипийн булцууг өөрчлөх замаар харж болно: Хэрэв дотроо тунгалаг байдал нь тунгалаг байвал нэрэхийг зогсоож, дараа нь нэрэхийг зогсоох хэрэгтэй. Үүний дараа шийдлийг хөргөхөд хүргэдэг. Товчоо юүлүүрт шилжүүлэгчийг шүүхэд шилжүүлэхгүй. Дараа нь бүтээгдэхүүнийг хоёр жижиг хэсэгтэй чимэглэлээр угаана хүйтэн усШүүгчдэд шилжсэн, Шилэн доторх олон тооны дулаан бодисыг нүүлгэн шилжүүлэх, натри 4-5% -ийн натрийн гидроксидийг натри, натри натри Цууны хүчил нь Фенольфофтеин дахь бараан улаан өнгийн шүүлтүүрт нэмж оруулдаг, дараа нь 1-2 давалгааны хүчил нэмнэ.
Бучнер юүлүүр дээр шаргал элсээр хөхөж буй фенолфтейлин. Түүхий бүтээгдэхүүн нь ойролцоогоор 10 мл архинд халаахад шилэн шилийг шилжүүлж, уусгана. Халуун уусмал нь халуун архины шүүлтүүр дээр тунадасыг сорж, угааж цэвэрлэв. Архи, согтууруулах ундаагаар архаагаар нь архины араас тос дуслуудаас наалддаг. Шүүгчийг шаазангийн аяганд шилжүүлж, архины чухал хэсгийг арилгахын тулд халуун элсний усанд шилжүүлэв. Аяганы холимог нь 30 минутын турш зогсож үлдэх болно. Нэр муугүй өнгөгүй эсвэл цайвар шар өнгийн талстууд нь шүүлтүүрийн цаасан хуудасны хооронд хөрсөнд автдаг.
1.4.2 физик шинж чанарууд нь синтезийн бодисод ашигласан физик шинж чанарууд
Хүснэгт 1
Синтезид хэрэглэгддэг бодисын физик шинж чанарууд
| Нэр | Томъёо | гадаад төрх | Т пла, 0 s | T Kip, 0 s | дугаарны байдал |
|
| Ус руу | өөр |
|||||
| Фенолфтейлин | 20 n 14 o 4-ээс | Өнгөгүй эсвэл элсэрхэг өнгөт ромбик зүү, үнэргүй, агаарт тэсвэргүй | 261 | байх тохирох | Үр ашигтай уусгагч (0.0002 гр 100 гр ус) | Диэтил эфир, дунд зэргийн бие даасан эфир, мөн шүлтлэг шийдлүүдэд уусдаг. |
| Дэболол | 6 n 5-аас тэр | Өнгөгүй эсвэл ягаан өнгийн ромын зүү | 41-43 | 182 | Хүйтэн - дунд зэрэг Халуун - сайн | Агаарт сайн, агаарт, агаарт, агаарт, агаарт, глороформ, Глицерин, Сероуголланд |
| Phthalic anhydride | 8 n 4 o 3-аас | Цагаан ромын зүү | 130,8 | Баруун 284,3. | муутай | Агаарт, агаарт, хлороформ дээр |
| Хүхрийн хүчил | H 2 SO 4 | Өнгөгүй, наалдамхай шингэн, тааламжгүй үнэртэй | 10,37 | 330 | | урвалд давтдах |
| Натрийн гидроксид | Nahh. | Цагаан бүдгэрч, ромбик талстууд | 320 | 1378 | Дулааны хувилбараар уусдаг | Архи, глицерин, фенол, эфир, эфир, acetone |
| цууны хүчил | Ch 3 coxy | Өнгөгүй шингэн, хурц салхинд хийсэх | 16,6 | 118,1 | | Этант, эфирт |
| Давсны хүчил | Даагай | Шаргал шингэн шингэн нь агаарт тамхи татдаггүй үнэртэй | -15,35 | - | бОЛЖ БАЙНА УУ | Архиданд |
1.4.3 Усны ууртай нэрэх арга
Учир нь, синтезийн хэрэгжилтийг хэрэгжүүлэх явцад фенолыг хэрэглэснээс хойш фенофилляциллыг хэрэгжүүлээгүй бөгөөд энэ нь цаазаар авах арга хэрэгслийг авч үзэх шаардлагатай бөгөөд энэ нь гүйцэтгэлийн аргыг авч үзэх шаардлагатай болно.
Аюулгүй байдлын хоолой, нэрэх хоолойн трифтийг аюулгүй байдлын агент (250 мл) үйлдвэрлэсэн төхөөрөмж дээр үйлдвэрлэсэн төхөөрөмж (250 мл), термометр, шууд хөргөгч, шууд хөргөгч, хүлээн авагч. Хофан-ийн хавчаар бүхий резинэн хоолойгоор резинэн хоолойгоор дамжуулж буй усан онгоцны болон нэрэх тосгуурууд нь хачигттай холбогдож, элс ванн дээр халаана.
Цус харвалтын нэрэлт (нэрэлт): Халуун хөвөгч нь халуун хөвөгч колбыг 100 мл буцалж буй усаар байрлуулна. Халаалтын уур амьсгал ба нэрэх колбо нь хариу үйлдэл хийгээгүй фэнолгүйгээр цуглуулдаг. Түүний дэргэд байгаа нь чипийн булингарыг нотолж байна. Туршилтыг булшлах нь ил тод чип гарч ирэхээс өмнө юм. 
Сах зураг Холбоно Усны гатлага нэрэх төхөөрөмж
1- Аюулгүй ажиллагааны хоолой; 2 - Parcelocking хоолой; 3 - tee; 4 - хавчаар; 5 - уурын зуух; 6 - klaisen-ийн колбо; 7 - термометр; 8 нь либид процесс; 9 - ALLEEZH; 10 - хүлээн авагч; 11 - Багана халаагч; 12 - хавтанцар.
1.4.4 Халуун архи, согтууруулах ундаа хэтрүүлэн татах арга
Туршилтын хувьд дахин боловсруулалтыг дараах байдлаар гүйцэтгэдэг: Бодисыг дараах байдлаар дугуй хэлбэртэй колбонд байрлуулна, бага зэрэг уусгагчийг нэмдэг. Холимог нь хавтан дээр халаасан усан ванны доор халаана.
Ихэнх шингэний хувьд хэт халалт хийх хандлага нь тодорхойлогддог, тиймээс тэд хүчтэй цочролд буцалгана. Халаалтын эхлэхээс өмнө колбонд зайлуулахаас зайлсхийхийн тулд буцалгана.Рефлюксоор дамжуулан уусгагчаар аажмаар бодисыг аажмаар нэмж өгдөг.
Бодисыг бүрэн татан буулгасны дараа халаалтыг зогсоож, хольцыг усанд ороод усаар хөргөнө. Үүссэн бодисыг шүүж байна.
Ихэнх тохиолдолд хоёр үе шаттай Recrystallization нь бодисыг цэвэршүүлэх найдвартай арга юм. 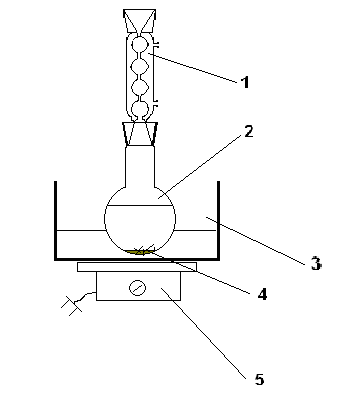
Фалбак.2b Дахин боловсруулах төхөөрөмж
1 рефлюкс; 2 - Бөөрөнхий доод колбо; 3 - усны өрөө;; 4 - буцалгана; 5 - хавтанцар.
1.5 Синтезис хэрэгжүүлэхэд аюулгүй байдал
Төвлөрсөн хүчилтэй ажиллахдаа 1.5.1 үндсэн аюул
Химийн түлэгдэлт нь химийн түлэгдэлт үүсгэдэг үед inorganical хүчил.Химийн түлэгдэлтийг цохисон төвлөрсөн хүчил, хүчтэй усны урсгалын шатсан газрыг угааж, дараа нь натрийн бикарбонатын 1% шийдэл (анхны тусламжийн хэрэгсэлд). Хэрэв хүчил цохих бол тэдгээрийг 1% натрийн бикарбонатын уусмал, нэрмэл өрөөний температурын усаар зайлуулна. Эмчид үзүүлэх тусламж хүсэх.
2. Төвлөрсөн давтамжийн хүчил нь хлоридын хлоридтой хамт хуйвалдаантай, энэ нь сайн идэвхтэй зүтгүүрийн дагуу ажиллах шаардлагатай. Хлоридын хордлого хэзээ хордлог бол шууд цэвэр агаарт гарах шаардлагатай болдог.
3. Хүчиллэг хүчиллэг нь хийнийг зогсоох хүртэл элсэн хүчиллэг, садар самуунтай карбонатыг өлгөхөд зайлшгүй шаардлагатай. Бүрэн төвийг сахисан усаар угаасны дараа элсэнд элсээр угаана. Угаалгын газрын асран дээр угааж, угаах (agno 3), хатаах шүүгээнд хатаах, хатаах кабинетад хатаах.
Усны гатлага нэрийн үед 1.5.2 үндсэн аюул
Нэрэх үед үндсэн аюул нь цахилгаан халаалтын төхөөрөмжийг ашиглахтай холбоотой байдаг (цахилгаан бамбай, багана халаагч).1. Дэлгүүр (та өөдөс ороомогоор утсаар утсаар ашиглах боломжгүй) Залгуур, Plate болон ElatoClux бие нь харагдахуйц гэмтээгүй байх ёстой.
2. Дулааны цахилгаан хангамжийн гадаргуугийн температурыг санамсаргүй байдлаар шалгана.
3. Сүлжээний цахилгаан тавилгыг багтааж, сэрээ, сэрээгээ оруулаад, сэрээ, нөгөө гараа бөглөнө үү. Унтраалга ашиглахын тулд халаалтыг тохируулах.
4. Дулааны шатаах тохиолдолд урт хугацааны Binding Peventing Peventing-ийг 0.5% Байнгын пиканяр хийх боломжтой, дараа нь ариутгасан боолттой, эмчтэйгээ нягтлаарай. 3 ба 4 градус шатаж байх үед ариутгасан боолт, эмчид хандана уу.
Халуун архи, согтууруулах ундаа хэтрүүлэн бодоход 1.5.3 үндсэн аюул
1. Нүдээ наалдамхай архины нийт хэмжээ нь 200 мл-аас хэтрэхгүй байх ёстой бөгөөд колбоны эзэлхүүний эзэлхүүний 1/3-оос илүүгүй байх ёстой.2. Усны ванны хэмжээ байх ёстой хэмжээнээс илүү Хавтангийн дулаан тусгаарлагч гадаргуу.
1.5.4 нь синтезид хэрэглэгддэг бодисуудтай ажиллах функцүүд
Бусдаас илүү химийн бодис Нэг арга замаар эсвэл өөр хортой. Тэдэнтэй хамт ажиллах нь эдгээр бодисыг бие махбодид нэвт норгохоос урьдчилан сэргийлэх арга хэмжээ авахад чиглэсэн байдаг.Синтез, болзошгүй бодисын үеэр Аюултай бодис хэрэглэх үед: Фенол, хүхрийн хүчил, цууны хүчил.
Феноол бол өнгөгүй (ягаан өнгөтэй), Тариалангийн үнэр, шинж чанартай талстууд юм. Ажлын талбай дахь MPC нь 0.3 мг / м 3 байна. Аюултай анги нь хоёр дахь нь юм. Фенол бүхий бүх ажил нь яндангийн кабинетад явагддаг. Хортой нөлөө: мэдрэлийн хор нь орон нутгийн ядаргаатай, нүүдлийн хүчтэй, нүүдлийн үр нөлөө, ерөнхий хордлого үүсгэдэг. Үхэх боломжтой. Нөхцөл байдал нь бодис нь орон нутгийн мэдээ алдуулалтыг үүсгэдэг гэсэн үг юм. Анхны тусламж: Хувцаслалтад ороход тэр даруй өөрчлөгдөж, арьсны тос, уусмалыг спирт 10-40% угаана.
SALECONCENCECTER нь HCL-ийн хоёр дахь аюулыг (MP / M 3 MG / M 3 MG / M-ийн Агаарын талбайн агааржуулагчтай, энэ нь барьцаалсан талбайд ажилладаг. энэ нь хлоридын хосыг онцлон тэмдэглэв. Хлоридын хлоридаар хордлого хийх үед цэвэр агаар гарахад шаардлагатай бөгөөд бусад аюулыг дээр нь зааж өгсөн болно.
Хүхрийн хүчил ( \u003d 1.84 гр / см 3) - PDK RZ \u003d 1 мг / м 3. Аюултай анги нь хоёр дахь нь юм. 5 секунд орчим дараа, даавууны эрч хүчтэй шингэн алдалт нь унасан хит эхэлдэг. Анхны тусламж: арьсны угаагч урсгал урсгал саармагжуулах замаар дараа нь.
Acetic хүчил - PDC RZ \u003d 5 мг / м 3. Аюулын ангийн гуравдагч 7. Хосууд амьсгалын дээд хэсэгт, 30% -иас дээш тооны бодисын массаас 30% -иас дээш жинтэй. Анхны тусламж: (хүхрийн хүчил, гидрохлорын хүчилийг үзнэ үү).
1.6 уусмалын шинж чанар
Уусмалын шинж чанар дахь тусгай газар нь диэлектрик тогтмол байдаг. Сүүлийнхоо давуу талтай харьцуулбал электростатик хүний \u200b\u200bэнгийн шинж чанаруудтай холбоотой бөгөөд ингэснээр DielEctic тогтмол нь уусмалын туйлшралын туйлшралтай холбоотой юм. Энэ талаар та нар уусгагчийн макроскопийн нэвчилтийг яг таг харуулсан нь харьцангуй диэлектрик тогтмол гэж нэрлэгддэг зүйлийг тодорхой мэдэх нь чухал юм.
r. = 0 /
0 - вакуумын диэлектрик нэвчилт.
Диэлектрик тогтмол нь цэнэглэгдсэн конденсерийн хоёр хавтангийн хооронд уусгагчийг байрлуулж шийддэг. Уусгагч, e-ийн хоорондох цахилгааны талбайн e-ийг вакуогоор хэмжигдэхүүнтэй харьцуулахад буурч байна. E 0 / нь уусгагчийн диекекцийн нэвчилт юм. Хэрэв уусгагч молекулууд өөрсдийн байнгын диполь мөчгүй бол гадны талбарын нөлөөн дор, интрамолекулын нөлөөн дор, интрамолекулын төлбөрийг өдөөгдсөн диполь хэлбэрээр тусгаарладаг.
-Аар / -оор цаасны дүрэм Тогтмол эсвэл өдөөгдсөн диполь бүхий молекулууд тодорхой байдлаар чиглэсэн байдаг; Энэ үзэгдлийг туйлшрал гэж нэрлэдэг. Туйлшралын түвшин өндөр байх тусам цахилгаан талбайн хүч чадлын улмаас хүчтэй байдаг. Үүний улмаас, Диэлектрик тогтмол нь төлбөр, өөрийн дүрийнхээ чиг баримжаа тусгаарлах чадвартай шууд холбоотой байдаг.
1.6.1 физик шинж чанар дахь уусгагчийг ангилах.
Диэлектрик тогтмол (DP) нь e нь хамгийн чухал хүчин зүйлүүдээс хамгийн чухал хүчин зүйлүүдийг хэлдэг хүчтэй нөлөө Шийдэлд тохиолдсон үйл явцын шинж чанар дээр.
Хувь хүний \u200b\u200bуусмалын DP нь бие даасан уусгагчдын утга нь маш чухал хязгаараас ялгаатай байдаг. DPINEVERING-ийг DESTINGERING-ийг DEPVERS-ийн төгсөлтийн талаар тодорхойлж, бүх зүйл тодорхойлогдоогүй, тууштай байдаг. Өндөр DP-ийн уусмалыг туйлш гэж нэрлэдэг тэр ч байтугай өндөр хэдийгээр шон, Хэдийгээр хэлдэг боловч "туйлшрал" гэдэг нэр томъёо нь Diar-ийн молекулыг in-ийг илэрхийлдэг, I.e.e.-ийн молко, бичил сэргэж чадахгүй байна.
Гэсэн хэдий ч энэ нь -ийг -ээр дагаж мөрдөж байгаа онолыг -ээр дагаж мөрддөг. Эдгээр утгууд өөрчлөгдөх шинж тэмдэг ажиглагдсан. Нэмж хэлэхэд, Диполь мөчний хувьд уусгагчийн шинж чанарын хувьд тэдний молекулууд "Диполь" нэр томъёотой (μ0) ба "μ) (μ \u003d 0) уусмал.
Бага туйлшралууд нь уусгагч, DP нь \u003d l, 8ch2-тэй, \u003d 12ch. Эдгээр нэлээд дур мэдэн сонгогдсон интервалд тийм ч их байдаггүй, гэхдээ нөхцөл байдалд ихээхэн хамааралтай байдаг.
Маш сайн тогтсон онол, үл тоомсорлож, DP ба DIPOLE-ийн хоорондох харилцаа, бие даасан шингэний мөч нь ба μ-ийн хоорондох утгагүй параллель . Диполлелелийн эсрэг (гинж биш гинж) нь нэг молекулын мөчний мөчний мөчний мөчний мөчний мөчний мөчийг дусалж, шингэний буурцагт хүргэдэг. Тийм учраас харьцангуй том хэмжээтэй диполь бүхий молекулууд үүссэн шингэний DP нь нэлээд бага байж болно.
Бүтцийн шинж чанарууд нь уусгагчийн туйлшралд ихээхэн нөлөөлдөг. Бүтэцтэй уусмал, дүрмээр бол өндөр DP-тай байх.
Диэлектрик тогтмол, Хомен-Чулуугийн химийн бонд үүсэх нь хувь хүний \u200b\u200bэнергиээс хамаарч хувь хүний \u200b\u200bшинж чанарыг тодорхойлдог хамгийн чухал хүчин зүйлүүдийн нэг юм. Сүүлийнх нь реактив харилцан үйлчлэлээр тодорхойлогддог бөгөөд энэ нь хязгааргүй их хэмжээгээр хамаарна. 1,1 n d, түүнчлэн Диполь мөч, мол ба молийн хэмжээ?:
E r \u003d. 
Хүснэгтийн хүрээний диполын молекулын реактив харилцан үйлчлэлийн утга 1-р хүснэгтэд өгөгдсөн.
М.ВАПАРРАВИВИЙН ХИМЭЭРИЙН МОЛТЕРИАЛГА АРМИ-ийн реактор Улсад зориулсан рееектузи талбарыг химийн бүтцээр үүсгэх нь химийн бүтээнтн дүрслэл шинэчлэлтүүд үүсгээс гаргахгүй гэсэн үгийг хэрэгжүүлэхэд хүргэдэггүй. Сүүлчийн тогтвортой байдал нь реактив талбайн энерги нэмэгдэхэд буурдаг.
Реактив талбайн энерги нь нэг төрлийн инженерийн бие махбодийн шинж чанарыг тайлбарласнаар, эсвэл үнэ цэнээр нь уусмалыг ангилахад тусгайлан тайлбарлаж болно - Er. .
Мэдээжийн хэрэг, молекулууд нь Di-Flece агуулаагүй бүх сорилт нь реактив бус анги байх болно шингэн. Интервал дахь реактив талбайн энерги бүхий уусмал - Er. = 0H5 KJ®OL -1-ийг идэвхтэй болгохын тулд бага зэрэг идэвхтэй, e e \u003d 5h15 kj mole -1 - e r mol mol mol -1 MOR 25 KJ нь анги юм Өндөр реактив уусмал.
Дүрмээр бол электролит, электролит, электролит, электролит, электролитыг сайн уусдаг бөгөөд энэ нь бусад ангиудын аль алинд нь илүү сайн байдаг. Энэ нь өндөр хэлбэртэй уусгагчийг DP болон DIPOLEMEME-ийн өндөр үнэ цэнэтэй хослуулсан гэдгийг тайлбарлана.
Хр. 2
298.15 K дээр зарим уусгагчийн реактив талбайн энерги.
| Утгагч | -E r, kj mol -1 | утгагч | -E r, kj mol -1 |
| Гүргээгч | 2,9 | Метил ettyl ketone | 3,4 |
| Ацетон | 9,1 | Шоргоолжны хүчил | 5,2 |
| Ацетонит | 20,9 | Нитробензен | 17,1 |
| Butyl архины | 2,9 | Nitromeeteta | 17,5 |
| Ус | 18,6 | Пиридин | 5,7 |
| Hexen-1. | 0,15 | Пропиленекконат | 43,8 |
| N, n-dimetylacetamide | 15,8 | Сахилгын архины | 3,6 |
| Диметил Дульфоксид | 6,4 | Тайланд | 0,05 |
| Диметилформамид | 19,5 | Цууны хүчил | 3,7 |
| Dioxan | 0,07 | Тетрахидрофуран | 2,9 |
| 1.2 - Дихлортейн | 4,2 | Хлоробензен. | 1,8 |
| o - xylene | 0,12 | Этил ацетат | 2,45 |
| n - xylene | 0,05 | Intylene glycol | 8,9 |
| N-метилкетамид | 24,1 | Хийг, зөрчил | 4,7 |
| Метил хэлбэртэй | 4,0 |
Наалдамхай байдал (илүү нарийвчлалтай, уян хатан хүчин зүйлээр ) шингэнийг 10 -2 pa s-тэй бага хамтлаг болгон хуваана.
Тодорхой цахилгааны дамжуулалтаар шингэн, шингэн нь "дамжуулагч" -тай хамт "дамжуулагч" шингэнийг -ээр хуваана ойролцоогоор 10 2 - 10-1 -1 см · M. -1 ба түүнээс дээш; "Дунд зэрэг дамжуулагч" - 10 -1 - 10 -4 ба C 10 -4 см. MM -1 нь "дамжуулагч бус" харьяалагддаг.
Буцалж буй температурыг ангилах уусмалыг ангилдаг. (1 50 0 сек) -д хуваагддаг.
Ууршуулах чадварыг ууршуулах, харьцангуй масштабаар харьцангуй масштабыг ууршуулах дулаан дээр үндэслэн санал болгож байна. Тиймээс дэгдэмхий (харьцангуй хэлбэлзэл 35) уусмалыг ялгаж салгадаг. Хэрэв та ууршилтыг шууд ууршилт хийх дулааныг удирдан чиглүүлбэл, дараа нь n-ийн тэжээлийн дулаанаар тодорхойлогддог уусмал Хүснэгт 3.
Dielectric тогтмолуудаар уусгагчийн ангилал
| Бага зэргийн түр |
|||
| Утгагч |  r. r. | Утгагч | r. |
| Ус | 78,30 | DMF. | 36,71 |
| Intylene glycol | 37,7 | Бензонитрилл | 26,20 |
| Метанол. | 32,66 | Нитробензен | 34,78 |
| Dmso | 46,45 | Глицерол | 51,7 |
| Сул туйл |
|||
| Цаг | 7,58 | Acetic anhydride | 20,7 |
| Диетил эфир | 4,20 | Butanone - 2. | 18,51 |
| Ацетон | 20,70 | Пенттантон - 2. | 15,38 |
| Этилийн этилийн. | 24,55 | Пиридин | 12,91 |
| Цууны хүчил | 6,17 | Метил ацетат | 6,68 |
| Propanol - 1. | 20,45 | Cyclohexanone | 16,10 |
| Butanol - 1. | 17,51 | Спам | 8,95 |
| Изоамил архи | 15,19 | Хлороформ | 4,81 |
| Гүргээгч | 6,71 | Эмилови архи | 13,9 |
| Ту яриа дугуй |
|||
| 1.4 - DIOXAN | 2,21 | Cyclohexane | 2,02 |
| Трихлоретилен | 3,42 | N - Пенттан | 1,84 |
| Бенненз | 2,27 | Нүүрстөрөгчийн салиа | 2,64 |
| Тайланд | 2,38 | Нарийн дэлгэг | 3,78 |
| Тетрачлорометрь | 2,23 | diethylcarconate | 2,82 |
| Тритетикин | 2,42 | ||
| h - геетан | 1,92 | ||
| h - hexane | 1,88 | ||
1.6.2 Химийн шинж чанарууд дээр суурилсан уусгагч системийн системүүд
Химийн шинж тэмдгүүдийн хамгийн их уусгагч системийн хувьд химийн шинж тэмдгүүдийн хамгийн их уусгагч систем нь тэдний хүчиллэг шинж чанарыг харгалзан үздэг. Тиймээс хамгийн их ерөнхий систем Уусмалын ангилал нь тэдгээрийг хоёр өргөн анги руу хуваах боломжийг олгодог
(Суурь) ба хүлээн авагч (хүчил), илт, үл тоомсорлосон уусмалын хуваарилалтын өөр нэг ангийг хуваарилах. Түншүүд бүрийг эдгээр ангийнхандаа өгөх, эсхүл уусгагч молекулыг өгөх эсвэл хүлээн авах чадвартай, уусгагч молекулыг өгөх эсвэл уусгагч, уусгагчийн аль алиныг нь татан буулгах шинж чанаруудаас хамаарна. Тийм учраас энэ ангилал нь хариу үйлдэл, уусгагчийн хэрэглээний асуудлаар уусгагчийн шинж чанарыг хамардаг.
Донорын уусмалын нийтлэг шинж чанар нь электрон дутагдалтай тоосонцор юм. Үүнтэй адилаар хүлээн авагч уусгагч нь илүүдэл электронтой хамт гурилыг шийддэг.
Хандивлагчийн олон төрлийн уусмалыг харьцангуй олон тооны элементүүд, эдгээр элементийн янз бүрийн олон тооны элементүүд, эдгээр элементүүдийн төрөл бүрийн элементүүдийг тодорхойлдог. Тиймээс энэ ангийн инжирийн төлөөлөгчид нь n-суурь (энгийн хэлбэр, архи, согтууруулах ундаа), 0-бааз, aldehdees, , R-BACE (Туршилт-, Трейлкил эсвэл Трейрил эсвэл алкилларлфффин) гэх мэт.
Хүлээн авагчийн уусмалыг протон болгон хуваадаг мөн aprotic.
Харуулсан функцээс хамаарч протолитик тэнцвэрт байдалд орж болох уусмалыг протофиликик (үндсэн) ба прото-бууруулдаг (хүчил). Хоёр функцийг ижил төстэй байдлаар илэрхийлдэг. (Архи, согтууруулах ундаа, кетонон) нь Amphipot гэж нэрлэгддэг.
Олон уусмалын молекулууд нь устөрөгч (n-) харилцаа холбоо үүсэхээс зайлсхийдэг. Үүний дагуу N-BOD-ийг бүрдүүлэхийн тулд уусмалын дагуу уусгах уусмалыг санал болгож байна.
Энэхүү ангиллын систем дэх анхны анги нь гурван хэмжээст n-Link сүлжээ байдаг. Энэ ангийн уусмал (ус, формат, форматик, хүхрийн хүчил, гликолис) нь маш өндөр DP, харьцангуй өндөр уян хатан байдал, наалдамхай урсгалын шинж чанартай байдаг. Дүрмээр бол энэ ангийн уусмал нь N-BOD-ээр дамжуулан гетеромолекуляр холбоог бие биедээ сайн уусдаг.
Хоёр дахь анги - n-Links-ийн хоёр хэмжээст сүлжээ бүхий шингэн. Дүрмээр бол энэ ангийн уусгагчийн молекулууд нь нэг гидроксилийн бүлэг (монохомийн согтууруулах ундаа, моносулятор, фонолик, фоноликат, фонолик, фоноль гэх мэт). Энэхүү бүлгийн гетеромолекулын холбоог бүрдүүлэх хүсэл эрмэлзэл нь ерөнхийдөө эхний ангийн төлөөлөгчид бага хэмжээгээр илэрхийлэгддэг.
Гуравдугаар анги нь молекулууд нь шингэн, хүчилтөрөгчийн атом, хүчилтөрөгч, хүчилтөрөгч, хүчилтөрөгч, хүхэр, хүчилтөрөгч, хүчилтөрөгч, флюфурин, extygur, extygein, extygen, suldygin, extygens, extygens, extygen, extygens, sulfur, oxtygen, extygen, extygens, extygens, extygen, extygen, extygens, extygens, extygen, exygurent, ProtonoDons-тэй холбоотой байдаг. Энэ анги нь aterers, ations, ations, ketones, aldehydes гэх мэт.
Дөрөвдүгээр ангид, молекулууд нь протонууд протонодонууд байж болно. Эдгээр нь хлороформ, дишигтоформ, дичиетейн, гэх мэт.
Тавдугаар анги нь хэвийн нөхцөлд H-BOD-ийг боловсруулж болох шингэнийг нэгтгэдэг шингэнийг нэгтгэдэг. Энэ бүлэгт алканес, нүүрстөрөгчийн тетрачлорлорид, цооролт, ингэж.
Паркер нь уусмалыг уусгах чадварыг сонгодог. Энэхүү ангиллын нэг хэсэг болох уусмалыг бүлэгт хуваана.
Apolar Primon - DP-ээс бага DP шингэн (
DIPARALAR APROTE - Харьцангуй өндөр DP WATES (\u003e 15) ба Dipole Moments (μ\u003e 2D) ,
n-BOD-ийг бүрдүүлэх чадвартай устөрөгч агуулаагүй байна. Энэхүү бүлгийн уусмалын төлөөлөгчид бол сульфурын төлөөлөгчид бол сульфур Диасзид, Нитрурезид, нитрозезид, нитромезен, нитромезид, acetoMente, acetoMentreile, acetoMentile, acetoMene, Acetylie Cockate, DMSO COOCOLE, DMSO COOCALE, DMSO-ийн
Устөрөгч нь электроген атомтай холбогдсон бүлэгт багтдаг протон-шингэн. Энэ бүлэгт багтсан нэгдэлүүд (карбоксилийн хүчил, архи, согтууруулах ундаа, архи, зүйрлэл гэх мэт) нь тодорхой холболтыг бүрдүүлэх чадвартай байдаг.
Ерөнхийдөө уусгагчийн уусгагч чадвар нь эхний бүлгээс гуравны нэгээс гуравны нэгээс өсч байна.
Bronstovad нь DIELECTRINE-ийн тогтмол, протогенийн хослолыг төдийг нь төдийг нь хослуулан хэрэгжүүлэхийг санал болгов. Эдгээр шинж чанаруудын дагуу тэрээр уусгагчийг найман бүлэгт хуваасан.
BRO "NSteda ангиллын нэг хэсэг болгон янз бүрийн бүлгийн уусгагч жишээ үйлчлэх болно: I - Ус, II - хүхрийн хүчил, шоргоолжны хүчил, III - Гидразин, ДМСО, IV - пропилен карбонат, nitrobenzene, ацетонитрил, Нитрометан, V - butanol ; VI - Шингэн Бромин ба Иодмоде; VII - Trietomamine, PIRIETINE; VIIIALING; VIIIAN - Hyiie - Hyxane - Chloie - Chlorene - Chlorobenzene.
Бронкендерийн дагуу ангилал нь бүлгүүд тус бүрийн уусмал дахь ууссан нэгдлийг урьдчилан таамаглах боломжийг олгодог. Ийнхүү, II бүлгийн уусгагч II-ийн уусгалт, баазын хүч III-ээс ихээхэн өндөр байна; III-ийн уусмалын уусмал дахь хүчлийн хүчний хүч нь VII-ийн Sopp-ийн уусмалаас илүү өндөр байдаг.
Хүснэгт 4.
Shroncender-ийн уусмалыг ангилах.
| Өмч хөрөнгө | Солонгийн хэлбэр |
|||||||
| Би.. | II. | Би | IV. | V. V. | Гүү | Вин | Viii. |
|
| DP. | + | + | + | + | - | - | - | - |
| Протогани | + | + | - | - | + | + | - | - |
| Тахилик | + | - | + | - | + | - | + | - |
* Тэмдгүүд + ба - эхний мөрөнд - эхний мөрөнд өндөр, бага DP хариу үйлдэл үзүүлдэг.
Мөн найман физик шинж чанарууд, MARPERSICES, MAREBODES, MARERSINEST, MALLERCAD-ийн PARMATION, ХӨДӨЛГӨӨНИЙ ТУХАЙ ХОРИУЛЖ, БУСАД ТОНОГ ТӨХӨӨРӨМЖ orbitals. Эдгээр шинж чанаруудыг нэгтгэснээр үүнийг есөн бүлгийн уусгагчдыг хуваахыг санал болгож байна.
1) Apricot Dipole (Жишээлбэл, acetonitrile, acetonitrile, нитроман, Нитрометан, ацетон, ацетон, ацетон, 1,2-dichlothane);
2) Apricot High-High-Ace (DMSO, DMF, DMA, DMA, DMA, Propylene Cocrate, Nitrobenzene);
3) Apricot High-High-Beat, өндөр туйлтай (Sulfolane, GMFTA);
4) Artomic бус туйлгүй (бензол, толуол);
Армоматик харьцангуй туйлшрал (хлоробензен, o-dichlorobenzene, acetophenOne);
Электрон Донор (Triethylamine, Ether, Ether, Dioxane);
H-бондын уусмал (архи, карбоксилийн хүчил);
n-бондтой хүчтэй холбоотой.
diethylene glycol, ус);
Тодорхойгүй функц (Servo нүүрстөрөгч, хлороформ).
1.7 ШИЛДЭГ ШИЛДЭГ ТЕХНИКИЙН ТЕХНИКИЙН ТӨЛӨВЛӨГӨӨНИЙ ТУХАЙ
1.7.1 Gravimetric уусмалын тодорхойлолт
Арга нь уусгагчийн тодорхой массыг уусгах бодисыг тодорхойлох нь (тодорхой уусдаг ` ) болон уусмалыг 100 граммыг татан буулгах чадвартай бодисыг тооцоолох. Арга нь тооцоологддог.Технологийн хэмжүүр дээр судалж буй бодисыг түдгэлзүүлэх (G 1 ` ). Уусгагч (g R) дээжийг баталгаажуулах. Хуурай шүүлтүүрийн массыг тодорхойлох (g 2). Уусгагч бодисыг тойрсон бодисыг тойрон хүрээлэх, хэрэв бодисыг бүрэн татан буулгахад үүнийг татан буулгахад нэмж оруулах шаардлагатай бол уусгагч (G 1) -ийг агуулсан бүх бодисыг тэмдэглэх шаардлагатай. Шүүлтүүрээр татан буугагүй бодисыг шүүлтүүрээр шүүж, нойтон шүүлтүүрийн массыг тодорхойлж, бодисын үлдэгдэл (g 3). Шүүлтүүрийг байнгын үлдэгдэлтэй байдаг. (G 4). ШИНЖЛЭХ УХААНЫ ТӨЛӨВЛӨГӨӨГИЙН ТУХАЙ ХУУЛЬ:
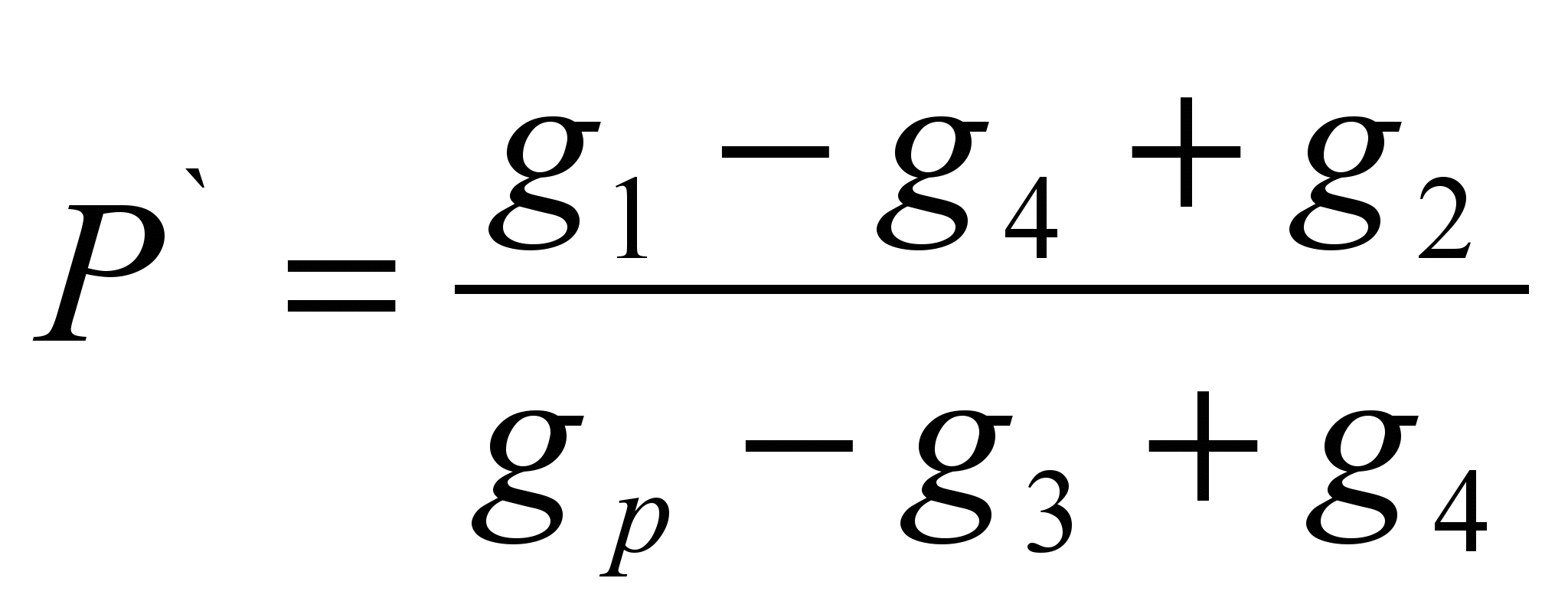
P \u003d r` · 100 (g / 100 гр)
Хүснэгт 5.
Зарим уусмал дахь фенолфтейлийн уусмал
| утгагч | аз | R. |
| Бага зэргийн түр |
||
| Ус | 0,0002 | 78,30 |
| Метил архи | 19,42 | 52,66 |
| Сул туйл |
||
| Хийг, зөрчил | 17,29 | 24,55 |
| Ацетон | 16,98 | 20,70 |
| хлороформ | 2,97 | 4,81 |
| Хэрүү бус |
||
| ксилен. | 0,19 | 2,43 |
| тайланд | 0,17 | 2,38 |
| бенненз | 0,16 | 2,27 |
1.7.2 электрохимийн арга.
1. Схемийн дагуу электролитын эсэргүүцлийг тодорхойлохын тулд COBAINT-ийг суулгацыг тодорхойлохын тулд суулгацыг тодорхойлохын тулд суулгацыг тодорхойлно уу (3-р зургийг үз).
2. Хэмжих саванд тодорхой концентрацийн усан үзмийн зайлсч, өгөгдсөн температурт термостатын ваарны усан үзүүрийг PATAL WATION шийдэлд оруулав. 15-20 минутын дараа усан онгоцнууд нь цэг дээр холбогдсон бөгөөд D нь суурилуулалтад холбогдсон байна.
3. Эсэргүүцсэн дэлгүүр, гар утасны тусламжтайгаар гүүрний үлдэгдэлтэй холбоо барих, утсаар ярих, эсвэл хамгийн багадаа ASCYLOGORAF дэлгэцэн дээрх хамгийн бага далайцтай. Нөхөн олговрын цэг нь үндэснээс нэг үзүүрээс нь тохиромжтой, дараа нь нөгөө талаас нь тохиромжтой. Хэмжилт ба дараагийн тооцооллын R x:
R x \u003d r 1 
Өөр өөр эсэргүүцэлтэйгээр 3-4 удаа давтана r 1. Хөдөлгөөнтэй холбоо барихтай ижил цаг үед луйварчдын төгсгөл хүртэл ойртох ёсгүй. Хэрэв хэмжилт хийхэд хазайлт 0.5% -иас бага бол үр дүнг нь сэтгэл хангалуун гэж үзэж, тогтмол хөлөг онгоцыг томъёо,
K \u003d. 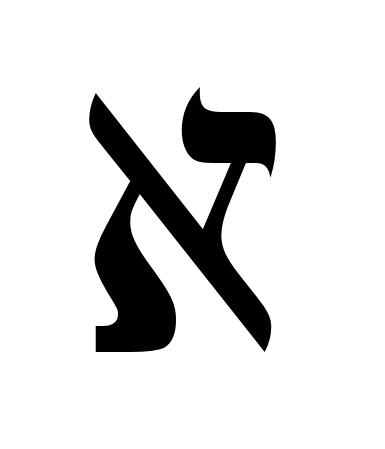 /
в Ч. В. =
R X.
/
в Ч. В. =
R X.
Хаана r x нь шийдлийн эсэргүүцэл юм; -
тодорхой цахилгаан дамжуулалт.
4. Бага хэмжээний давс нь 100 мл ус асгаж, залгуурыг нягт хаасан, залгуурыг нягт хааж, 20 минутын дотор тасралтгүй хаав. Үүний үр дүнд түдгэлзүүлэлтийг шилэн шүүлтүүрээр сорж, хур тунадасыг ханасан уусмалыг бэлтгэхэд ашигладаг. Үүний үр дүнд үүссэн уусмалыг цахилгаан дамжуулагчийг хэмжихэд цахилгаан дамжуулагчийг хөлөг онгоцонд оруулаад уусмалыг эсэргүүцсэний дараа.
=
к. /
R X. 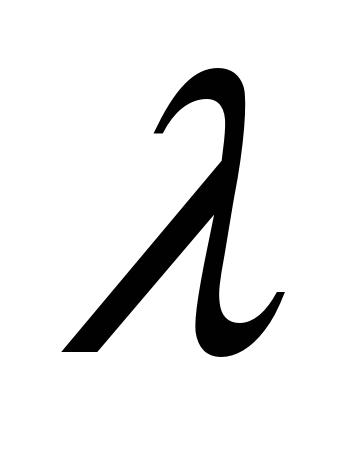 = /
С c.
= /
С c.
CHEACE нь CHEACE нь шийдлийн хэвийн байдал юм. Kg · eq / m 3.
Давстай уусмалаас хойш давсны агууламж бага байна, дараа нь \u003d . Тэгшитгэл дээр үндэслэсэн:
\u003d ( r - -аар / -оор ) /
Хаана r - давсны уусмалын тодорхой цахилгаан дамжуулагч.
Монововатор электролитын уусмалын үрэлт:
![]() = (C ) 2
= (C ) 2
6. Ширээн дээр тавих үр дүн:
| давс | t, c 0 | , сахаах | Эсэргүүцэл, өө. | К. | | | Хамт | L. |
|||
| R 1. | R 2 (ac) | R 3 (CB) | R X. |
||||||||
Хүснэгт 6.
KCI-ийн шийдлийн тодорхой цахилгаан дамжуулалт
| t, c 0 | 1 n kci. | 0.1 N. | 0.02 Н. | 0.01 N. |
| 10 4, OM -1 ° см -1 |
||||
| 0 | 654,1 | 71,5 | 15,21 | 7,76 |
| 10 | 831,9 | 93,3 | 19,94 | 10,20 |
| 14 | 906,3 | 102,5 | 21,93 | 11,21 |
| 16 | 944,1 | 107,2 | 22,94 | 11,73 |
| 18 | 982,2 | 111,9 | 23,97 | 12,25 |
| 20 | 1020,7 | 116,7 | 25,01 | 12,78 |
| 22 | 1055,4 | 121,5 | 26,06 | 13,32 |
| 24 | 1098,4 | 126,4 | 27,12 | 13,86 |
| 25 | 1118,0 | 128,8 | 27,65 | 14,13 |
| 26 | 1137,7 | 131,8 | 28,19 | 14,41 |
| 28 | 136,2 | 29,27 | 14,96 |
|
| 30 | 141,2 | 30,36 | 15,52 |
|
| 32 | 146,2 | 31,46 | 16,09 |
|
| 34 | 151,3 | 32,56 | 16,67 |
|
| 36 | 156,4 | 33,68 | ||
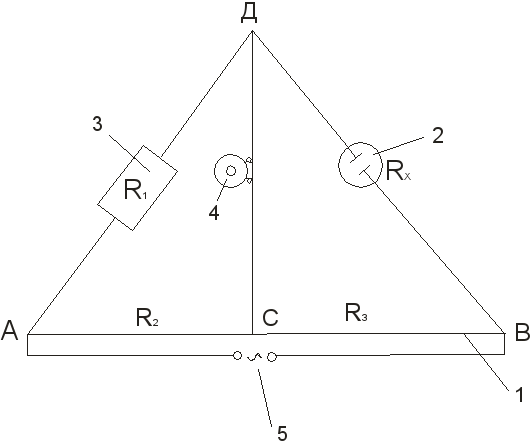
3-р зураг. Цахилгааны дамжуулалтыг тодорхойлох суулгалтын схем:
1 - шугам шугам дээр сунгасан утас; 2 - Улилцалттай савыг хэмжих; 3 - дахин ашиглах; 4 - бага түвшний утас; 5 - Одоогийн эх сурвалж.
1.7.3
Фоточитектроцалометрийн арга.
Арга нь гэрлийн шингээлтийг үндсэн эдлэлийн хуулийн үндсэн хуульд заасны дагуу аргыг үндэслэнэ.
Дэвшил
1. Гэрлийн оновчтой шүүлтүүрийг сонгох.
1.1. Хэмжих колбонд 25 мл газар:
Шийдэлийг хольж, энэ нь хамгийн тохиромжтой CUVETER-тэй хамгийн их хөнгөн шүүлтүүр бүхий сонгосон уусгагчтай харьцуулахад оптик нягтралыг хэмжинэ. Хэмжээ Cuvette зааж өгнө үү. Бид хэрэгслийн паспорт дахь Фек дээрх ажлыг хардаг.
1.2. Авсан өгөгдөл нь хүснэгтэд байна:
1.3. Миллиметр цаасан дээр, гэрэл шингээгч муруй a \u003d f (, nm) нь ажиллахдаа хамгийн сайн хэрэглээг хамгийн сайн ашигладаг.
2. График барих.
2.1. Цуврал стандарт шийдлийг бэлтгэ. Өмнөх шүүлтүүрүүдтэй хамт бэлтгэсэн цуврал цувралын цуврал цуврал тус бүрийн оптик нягтралыг хэмжих.
2.2. Хүснэгтийг тусад нь хийсэн шийдэл тус бүрийг тус тусад нь хүснэгтэд байрлуулах (доороос үзнэ үү).
2.3. Хүснэгтийн өгөгдлийн дагуу Millimeter цаасан дээрх хүснэгтийн дагуу A \u003d F (C), Phionphephthein-ийн уусмалыг уусмалаар тооцоол.
Фенольфефенааны уугуулийг фэнольфенааны уусмалыг судалж үзсэний дараа дээр дурдсан техникийг сонгосон. Боломжтой бол тэдгээрийг харьцуулж, уусах чадварыг ашиглах нь бидний лабораторийн нөхцөлд хэрэгжүүлэх хугацааг сонгосон.
2. Туршилтын хэсэг
2.1 Фенольфтена мужийн синтез
Синтезийг уран зохиолын тоймд заасан аргын дагуу явуулсан (1.4.1-р зүйлд).
| Үйлдэл | ажиглалт |
| 1. явсан: 5G -Pali Anhydrid (H.CH.D.A) | Цагаан талст нунтаг Ягаан, хугарсан талстууд |
| 2. урвалжуудын урвалж бодисыг хавтгай ёроолтой конвенцик колбонд (100 мл тутамд 100 мл), термометр гарын үсэг зурав. | Холиурын массыг бүрдүүлэв, хольцын жижиг халаалт үүссэн, жижиг халаалт гардаг (T? 37 0 C). |
| 3. Колбыг заагчийг элсээр халаахад халаана (температур нь 125 - 130 0-ийн хязгаарт байна). 1.5 цагийн турш халаана. | 45 0 ° C-ийн температурт, фенол хайлж, фэнол хайлж, феалик anhydride нь өрөмдлөгийн платемид үерт автдаг. 30 минутын турш халаалтын дараа (T? 130 0 C), нэгэн төрлийн өсөлт үүссэн - бөөрөлзгөнө хайлж байна. 1 цаг халаалтын дараа - цусны улаан өнгөтэй нэгэн төрлийн хайлалт. 1.5 цагийн дараа халаалт зогссон. |
| 4. Халуун хайлж, буцалж буй усаар галладаг, усны ууртай урвалд өртөөгүй (суурилуулах зургийн тоймыг харгалзан үзсэн нэрэлтийг үзнэ үү). | Халуун хайлж, Халуун хайлж, Халуун хайлж, Фенольфтейлин, баримал шар өнгө, баримал нь цайвар өнгөтэй, барималгүй хэсгүүдийг усанд сэлж эхлэв. 99 0 C. Turbid Chip (v \u003d 50 мл) -ийг даван туулах тохиолдол гардаг. 15 минутын дараа нэрэх, нэрэх нь тунгалаг нэрмэлийг дусалж эхлэв. |
| 5. Шимнасеалений уусмалыг хураангуйгаар шилжүүлэхгүйгээр шийдэлтэй шийдэлтэй шийдлийг гаргав. Гурван хэсэг хүйтэн устай, 100 мл тус бүрээр тунадас бороо оров. | Судалгааны 26 0 сек, уусмалын температур (v? 170ML) нь фенофффелин, бага зэрэг шаргал өнгөтэй. |
| 6. 15 мл-ийн дулаан натрийн гидроксидын уусмал (? \u003d 5%) шүүлтүүртэй фэнолфтен. | T NAOH? 42 0 S, Шийдлийн толбо болсон - Хар улаан. |
| 7. Харанхуй улаан уусмалыг шүүх. | Шийдлийн температур? 35 0 S шүүлтүүрийн шүүлтүүр дээр шүүлтүүрийг шүүж, нимгэн, ягаан цагаан, жижиг талст бодисын бодисыг шүүж, нимгэн, жижиг талстаар хийнэ (хамгийн их магадлалтай). Хамгийн их магадлалтай (хамгийн их үйлдэл нь phalalic anhydride хийгээгүй байх). |
| 8. Шүүлтүүрийг хэрхэн яаж (v? 50 мл) 5 мл-ийн цууны хүчил (k.), 1 мл-ийн хэсэг нэмэв. | Харанхуй улаан, улаан улаан-саарал цагаан, шавартай (Finaked) уусмалын уусмалын өнгө өөрчлөгдөж байсан. Уусмалыг дулаацуулах нь тохиолдсонгүй. Шийдлийн температур? 31-ний өдөр |
| 9. 2 дусал гидрохлорлик хүчил (k.) | Харааны өөрчлөлт Тохиолдоогүй |
| 10.Таны 1 цагийн турш зогсож байна. | Шилэн ёроолд шилжсэн нь тунадас, тунадасны дээд хэсэгт тунадас, тунгалаг, тод шийдэл, саарал цагаан өнгөтэй үр тариа. |
| 11. Үр дүнд хүрсэн хур тунадас. | Шүүлтүүр дээр цагаан саарал саарал кассети байна. М ll? 5.07 |
Нийт 5.07 гр нойтон хар тамхи.
2.2 Халуун архины дахин боловсруулалт
Recrystallization нь утга зохиолын тоймд заасан журмын дагуу хийгдсэн (1.4.4). Нэг давталт хийсэн. Төхөөрөмжийн зураг зурах нь утга зохиолын тоймыг 1.4.4-т дүрсэлсэн болно.
| Үйлдэл | Ажиглалт |
| Хипстер Фенолфтейлин (5.07 гр) колбонд байрлуулж, 50 мл 96% этилийн спиртийг дагаж мөрдөв. | Фунфттины бага хэсэг нь ууссан. Архи бага зэрэг үүлэрхэг. |
| Колбо нь сул буцалгахад халаана. Фенольфтфеин (0.5 мл) -ийг бүрэн татан буулгахад архи нэмсэн. V etoh \u003d 7 мл. | фенолфтейлин бүрэн ууссан байв. Архи нь зовлонтой юм. T Холимог \u003d 85 o c. |
| Холимог нь өрөөний температурт аажмаар хөргөнө. | t Холимог \u003d 19-ийн тухай C. Уусмалаас нь C. Уусмалаас бага зэргийн цагаан талстууд байсан. Шийдэл нь тунгалаг юм. |
| Дусалдсан талстууд санал болгосон бөгөөд шүүлтүүрийн цаасан дээр цаасан дээр хатсан усаар хатсан, шүүлтүүрийг угааж, угааж цэвэрлэнэ. | фенолфтеиныг агаарын талст хэлбэрээр олж авдаг цагаан саарал, нарийн ширхэгтэй. м (Фенольфтален) \u003d 4.08 гр Дахин эргэлтийн ургац 83.5% байсан. |
RECRYSTALLACE-ийн тооцоо:
ReCryStallization Fass:
W,% \u003d (m (феноффенен) Хатуу 100%) / m (Фенолффтен)
W,% \u003d  % = 83,5 %
% = 83,5 %
Синтезийн гарцыг тооцоолох:
0.0388 MOL PHENOLPHEPHEALEIN (теореттфена) эсвэл M \u003d 0.0338 MOL 318 г / mol \u003d 10.7 г.
Онолын онолоос гарах:
W \u003d  100 % = 40, 5 %
100 % = 40, 5 %
Тиймээс зарчимд олж авсан бүрэн тоо Фенолфтейнина (цаашид судлахад зориулж 4.08 гр). Синтезийг хүлээн зөвшөөрөгдсөн бүтээгдэхүүний гаралтаар гүйцэтгэсэн.
2.3 уусмалын тодорхойлолт
Фенолфтефалины уусмалыг тодорхойлох нь жийргэвчний аргыг граниметрийн аргаар гүйцэтгэсэн (1.7.1-ийг үзнэ үү).
Хлороформ, бензол, ксиленийг уусгагчаар сонгосон. Уран зохиолын мэдээллээр (CMTALSTSTA 5), Phenolphthalene нь феноффтфелины одоо байгаа массын хувьд хүлээн зөвшөөрөгдсөн уусмалтай байдаг. Фенолфтенеен нь маш бага уусмалтай тул ус ашигладаггүй тул (100 гр тутамд 10-19 гр). Энэ нь спиртийг хэрэглээгүй, фенолфтфелийн гадаад төрхийг архи, согтууруулах ундаагаар маш сайн уусдаг бөгөөд бодисын томоохон хэрэглээг шаарддаг. Тодорхойлолтыг 21 ± 1 ° C (шингэн фазын температур) хийсэн. Хүсэл эрмэлзэл нь 30 ± 1 минутын турш, хүчтэй хутгана.
Тооцооллын томъёо:
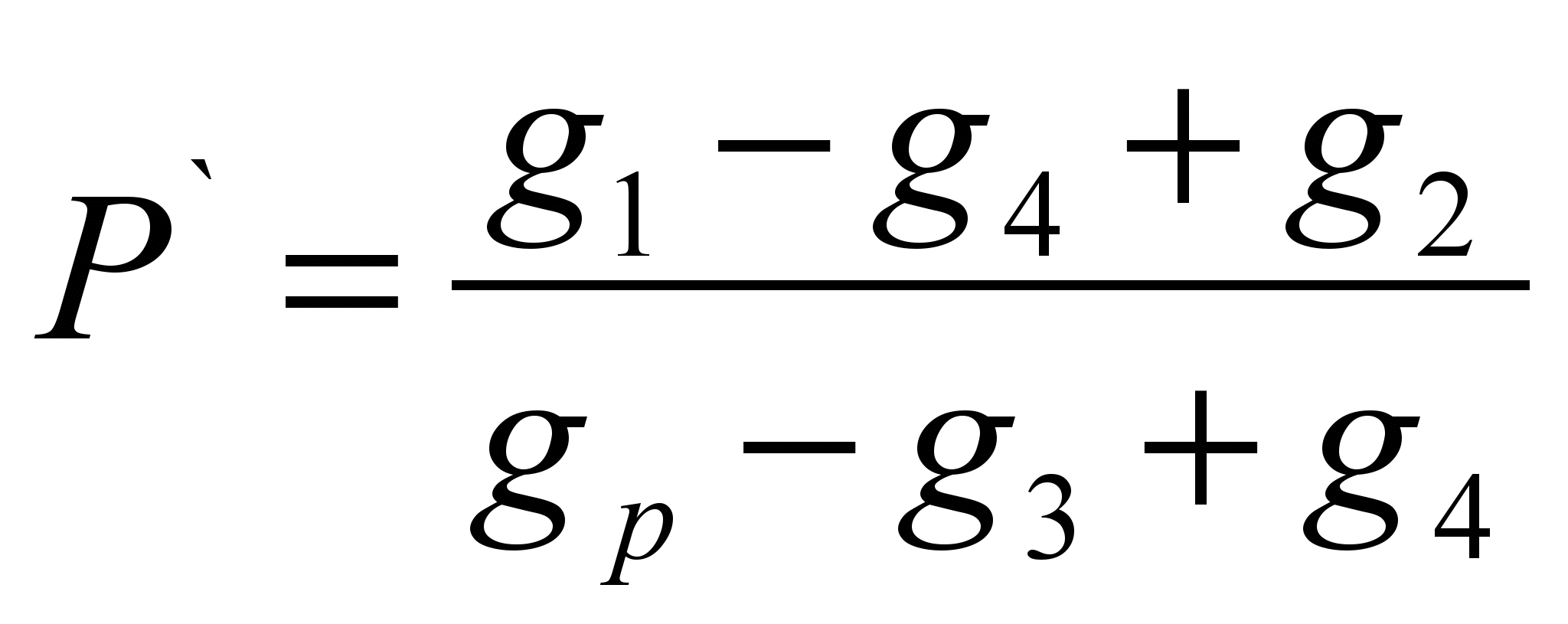 ;; P \u003d r` · 100 (g / 100 гр)
;; P \u003d r` · 100 (g / 100 гр)
Хаана, g 1 бол Фенолфтфтенегийн чанамал, r;
G 2 - хуурай шүүлтүүр, r;
G 3 - Фенольфтфелийн үлдэгдэлтэй нойтон шүүлтүүрийн масс, r;
G 4 - Фенольфтейлийн үлдэгдэл бүхий хуурай шүүлтүүр, r;
G P - Уу ганцаараа зууш, R;
P - уусмал, g / 100 гр шийдсэн;
P`- тодорхой уусмал, g / 1 гр.
Тодорхойлолтын үр дүн:
P (Фенолфтфенен / хлорофен) \u003d (3.0 ± 0.03) G / 10033) G / 100 гр хлороформ; Чи? \u003d 1%.
P (Фенольфталь / xylene) \u003d (0.22 ± 0.21) G / 100 гилийн; Чи? \u003d 6%.
P (Фенолфтегал / Бензен) \u003d (0.19 0.11) G / 100 0.1) G / 100 гр бензол; \u003d 6%.
Туршилтын дагуу нэгтгэсэн ширээ, хуваарь барьсан.
Хүснэгт 7.
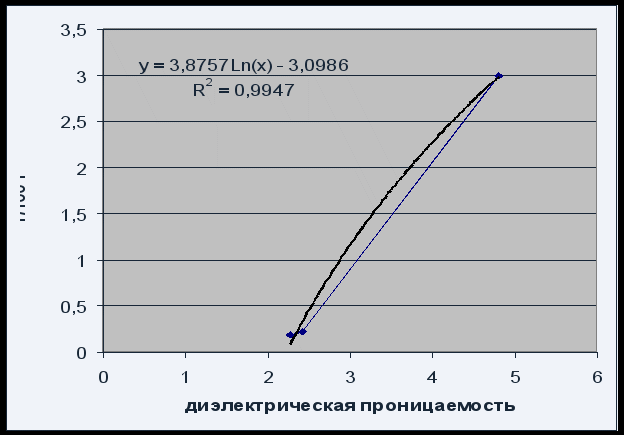
Зур \u003e.4. Уусгагчийн Dielectic-ийн Dielectical-ийн уусмалаас уусах чадвараас хамаарал
Уусгагчийн уусгагчийг уусгах уусмалаас хамаарал нь Lountricuct-ийн уусмалыг логарифмын тэгшитгэлээс тодорхойлж болно.
Фенолффелеин уусах уусмалыг уусгагчаар уусгах уусмалыг уусгах чадварыг нэмэгдүүлдэг тул фэнолфтефенеенийн тугалганы нэгдлийг нэмэгдүүлдэг.
Байгуулах
Ажлын явцад 26 утга зохиолын эх сурвалжийг дүн шинжилгээ хийсэн. Феноол, Фенотикатын харилцан үйлчлэлийн урвалын талаархи ерөнхий байрлалыг тайлбарлав. Синтезийн техникийн тоймыг хянасан (нэг арга олдсон (нэг арга олдсон, өөр өөрөөр хэлбэл, өөр өөр утгатай. Энэ техникийн синтезийг хажуугийн үйл явцын хувьд төвөгтэй биш юм. Үндсэн аюулыг синтезийн үеэр тодорхойлж, бодисын хэрэглээний эргэлтэд тодорхойлно. Уусах чадварыг тодорхойлохын тулд сонгосон аргууд. Хлороформ, ксилен, Бензенийг уусах чадварыг тодорхойлохын тулд уусмалыг сонгосон.
40.5% -ийн ургац бүхий феноольфтейлийн синтез. Синтезийн нөхцөл байдал, цэвэрлэгээ, хуваарилалт нь техникийн мэдээллийг үнэн зөв дагаж мөрдөж байсан.
Фенольфтейлины уусмалыг (жийргэсний тодорхойлолтоор): 3.00 ± 0.00 ± 0.0G Хлороформ, 0.00 ± 0.0G Хлороформ, 0.00 ± 0.0G chloroform, 0.00 ± 0.0G Хлороформ, 0.00 ± 0.00 гр ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G, 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G ± 0.0G.
Фенольфтейлины уусмалыг уусгах уусмалын уусгагчийг уусгах чадварыг нэмэгдүүлдэг. Фенолффтене нь Aiolleneen нь aiolleneen-ийг баталж байгааг баталж байна.
Ашигласан уран зохиолын жагсаалт
1.Arrontomeob A.E. Органик химийн чиглэлээр лабораторийн ажил. - м .: Гэгээрэл, 1977. 230 p.2.Атакхова л.и., kriveysone A.P. Органик химийн талаар семинар. - M.: MIR 1990. 180. 180 P.
3. Бишотын E. Шалтгагч бодисууд. - M .: MIR, 1976. 356 х.
4. Буллер К., Пирсон D. органик синтез. М .: Өндөр. ШК., 1973. 340 p.
5.GERASAMIME YA.I. Шийдлийн термодинамик. - M.: ED - Москвагийн муж улсын Их Сургуульд 1980.70.70 P.
6.Хэрэгтний S. S. S. S. органик химийн Хими / с. S. Gity, A. I. Нүд, A. Ivanov. - M .:99 ба 1991.
7. Голодников G.V. Органик химийн талаар семинар. - М. Хими, 1978. 160c.
8.grandberger I. I. I. I. ДЭЛГЭРЭНГҮЙ АЖИЛЛАГААНЫ АЖИЛЛАГАА, СЕМИНАР ХИЧЭЭЛИЙН ХӨГЖИЛ: Суралцах тэтгэмж. их сургууль. - 4-р ED., Перераб. ба нэмэх. - M .: 2001 оны уналт.
9.ivanov v. G. G. G. GEAR SEARSHOP: Суралцаж байна. Судалгааны гарын авлага Илүү өндөр. Ped. судалдаг. Байгууллага / дотор. G. Ivanov, O. N. Geva, yu. G. G. G. GAVEROVA. - M .: Нийтлэх төв "академи", 2000.
10.carapetyanteAndz M.K. Химийн үйл явцын талаархи танилцуулга. - м .: Өндөр. ШК. 1975. 280 S.
11.Кирилин v.a. Шийдлийн термодинамик. - M.: ENERMIA, 1980. 80 S.
12.Кокан v.b. Уусмалын гарын авлага. - M .: L. L. L. ХУУДАСНЫ АКАДЕРИЙН АКАДИНГИЙН АКАДИ-г 1961. 300 P.
13.Levina R. ya. Органик химийн чиглэлээр практик ажил. - M .: ХИМИЙН ХИМИЙН ХИЧЭЭЛ.
14.Рикинг: Органик химийн чиглэлээр практик ажил. - M.: MIR нь 1979 - T.2.
15. СОНГОЛТ A. A. A. A. A. ARMICE Хими: Их сургуулиуд / A сурах бичиг. A. PETROV, H. V. V. BALIAN, A. TROIDKCHKO. - 5-р ED., Перераб. ба нэмэх. - SPB :: Иван Федоров, 2002 оны.
16.Rayhard K. Органик химийн бодис дахь уусмал, хүрээлэн буй орчны нөлөө. - М .: 1991. 1991. 182 p.
17. Органик химийн химийн хичээлд лабораторийн ангид лабораторийн ангиудад: их дээд сургуулиудын тэтгэмж / n. N. Artemieva, V. L. L. L. L. L. L. L. L. Beloborodova, S. Ed. N. A. TUBAVKINA. - 2-р Ed., Перераб. ба нэмэх. - M .: 2002 оны уналт.
18. Амжилт органик нэгдэл: Лавлах / ed. A. A. Poykhina. - L .: ХИМИЙН ХИЧЭЭЛ, 1984.
19.SMOLINA T. A. A. A. ACTICE CINTATION дээр практик ажил: Жижиг семинар / t. A. Smolina, N. V. VASILYEVA, N. B. B. KEPLESKYA. - 2-р Ed., Перераб. - М .: Гэгээрэл, 1986 он.
20.FRAW Химич / Эд. B. N. N. N. NIKOLSKY ба бусад. - L. L .: ХИМИЙН ХИМИЙН ЗАСГИЙН, 1964.
21.Стромберг А. Г. Химийн химийн бодис: судалгаа: Химийн хувьд. Мэргэжилтэн. их сургууль / а. G. Stromberg, D. P. Sechchenko; Ed. A. G. Stromberg. - 5-р Ed., Үйлдэл. - M.: VS, 2003 он.
22.traven v. F. F. органик хими: Их сургуулиудын хувьд сурах бичиг. - M.: ICC-ийн "Академнейн", 2004. - T.1.
23.физик хими. 2 kn. Тээ Навир 1. Бодисын бүтэц. Термодинамик: судалгаа. Их сургуулиуд / k-ийн хувьд. S. KRASNOV, N. K. K. VOROBYOV, I. \u200b\u200bI. I. GRNNEVEV, ETC гэх мэт. Ed. K. S. KRASNOWA - 3-р ED., Арын - M.: VS, 2001.
24. Fials yu.a. Химийн процессын хяналтын хяналт гэсэн үг. - L .: 1990 оны Хими, 1990. 240 сек.
25. Химийн нэвтэрхий толь бичиг / ED. I. L. L. L. Knunyanta болон бусад. - М. Зөвлөлт нэвтэрхий толь бичиг, 1983.
26.hramkina m.n. Органик синтезийн семинар. - M .: 1985 оны Москод муж улсын их сургуулийн байрны байшинг хэвлүүлэх. 473 p.
Эмпирик Фенолфтелийн томъёо: C20H14O4. .
Фенольфтален гэж юу вэ?
Wikipedia-ийн дагуу 4,4'-dioxiphtalophenope эсвэл 3,3-BIS- (4-Hydroxphenl) Phthalide төлөөлдөг хүчиллэг үндсэн үзүүлэлт .
Ийм бодисууд шиг lacmus, фенолфтена, метилован Шийдлийн хүчиллэгийг тодорхойлох химийн чиглэлээр өргөн хэрэглэгддэг.
Устгаагүй нь усгүй бол усанд уусдаг тунгалагалал юм. Гэхдээ энэ нь архи, согтууруулах ундаа хэрэглэдэг диетил эфир Байна уу. Бодисыг синхрончлож болно фенол. ба phthalic Anhydrida Конденсацийн урвалыг ашиглан ашиглан Цоо ххлорид цахилгаан тэгэж катализатор (Та одоо ч анхаарлаа төвлөрүүлж болно Хүхрийн хүчил ).
Хүчиллэг орчинд энэ бодис ( р ПНХ 0-ээс 3-аас 3) нь улбар шар өнгийн tint олж авдаг. Сул дорой байдал, төвийг сахисан хэвлэл мэдээллийн хэрэгсэлд ( р ПНХ 4-ээс 7 хүртэл) уусмал нь түүний өнгийг өөрчлөхгүй. Фенольфтейлиныг ашиглан та шүлтлэг орчныг таних боломжтой. Хэрэгсэл нь Crimson өнгийг уусмалаар олж авдаг тул р ПНХ энэ нь 8-аас 10 ( шүлтлэг rr). Хэрэв үнэ цэнэ устөрөгчийн үзүүлэлт 11-ээс 14-ээс 14 хүртэл, үзүүлэлт нь эмийн өнгөнд нөлөөлөхгүй. Фенолфтеинийг ашигладаг гадна Хүчинтэй хийн гаргаж цэнэ -аар / -оор аналитик хими Архи согтууруулах ундаагаар ууссан бодисыг ихэвчлэн хэрэглэдэг.
Мөн Фенолфтейлиныг анагаах ухаанд өргөн хэрэглэгддэг. Юу вэ Цэвэршил Чи? Энэ нь фэнольфтенатай ижил утгатай. Өнгөрсөн зууны үед уг бодисыг идэвхтэй байдлаар идэвхтэй ашигласан. Мансууруулах бодис нь гэдэсний перистатуудыг идэвхтэй өдөөдөг. Одоо Purgen-Loxivative нь бие махбодид хуримтлагдаж, бөөрний ажилд сөргөөр нөлөөлөх чадвартай байдаг.
фармакологийн нөлөө
Laxative.
Фармакодамик ба фармакокинетик
Фенольфтейлин, энэ юу вэ?
Purgen бол хүчирхэг laxative юм. Түүний үйл ажиллагааны механизм нь бэхжүүлэхэд суурилдаг перисталиктик гэдэс. Энэ нь зоосны бодисын чадвараас болж тохиолддог натрийн калсиум atfas Гэтгэлийн adenly cyclase нэмэгдэх болно биосинтез Байна уу. Бодис нь синапсуудыг өдөөдөг синапууд болон гэдэсний хананы төгсгөлийг өдөөдөг ус-электролитын үлдэгдэл -аар / -оор Zhkt. Шингэн хуримтлагддаг.
Эхний хүлээн авсны дараа эхний хүлээн авсны дараа 24 цагийн дотор тохиолддог. Бодис нь бие махбодид хуримтлагдах шинж чанартай байдаг бөгөөд бөөрөнд цочромтгой нөлөө үзүүлдэг кокеногийн шинж чанар.
Ашиглах заалтууд
Энэ бодисыг агуулсан бэлтгэлийг агуулсан бэлтгэл нь архаг бүхий лаксатик хэлбэрээр ашигладаг.
Эсрэг заалтууд
LAXION PUNGEN нь эсрэг заалттай байдаг:
- бөөрний өвчний хувьд;
- Өвчтөн С. гэдэсний түгжрэл ;
- фэнолфтейлинтай;
- Өвчтөний шинж тэмдгийн цогцолборт өвчтөн илэрсэн тохиолдолд " хурц гэдэс ”.
Мансууруулах бодисыг удаан хугацаанд ашиглах боломжгүй. Ахмад настнуудын эмчилгээнд онцгой анхаарал хандуулах ёстой.
Сөрөг нөлөө
Purgen шахмал нь дараахь зүйлийг өдөөж болно.
- зөрчлийн улмаас хурдан зүрхний цохилт ус ба электролитийн үлдэгдэл ;
- альбуминурия ;
- сүйрэл ;
- цусан дахь калийн түвшинг бууруулах;
- шар өнгийн өнгийг шар эсвэл хүрэн хүртэл өөрчлөх;
- арьсны тууралт ба.
Purgen-ийн заавар (арга ба тун)
LAXIONION нь таблет хэлбэрээр таблет хэлбэрээр гардаг.
Фенольфтеин ашиглах заавар
Дунджаар, насанд хүрэгчдэд зориулсан өдөр тутмын тун нь 100 мг юм.
Хүүхдүүд өдөрт 50-200 мг мөнгө, нас, жиннээсээ хамааран 50-200 мг томилогдсон.
24 цагийн дотор авах боломжтой бодисын дээд хэмжээ - 300 мг.
Эмчилгээний явцыг мэргэжилтэн томилсон. Энэ бүрэлдэхүүн хэсгүүдийг агуулсан бэлтгэл нь удаан хугацаанд авах боломжгүй.
Хэт их
Эм нь шалтгаан болдог Hemorrhoidal цус алдалт , мэдэгдэхүйц бууралт, хүртэл сүйрэл , шээсний уураг гарч ирэв. Экспортлох үед эмчид хандахыг зөвлөж байна.
Харилцан ажиллагаа
Фенольфтейлин нь параси саатлыг параллель хийж чадвал бие махбодийн саатал руу хөтөлдөг потассибэблингинг Дижитик .
Борлуулалтын Ндарар
Жорыг шаардлагагүй.
Хадгалах нөхцөл
Пенольфтеин дээр суурилсан бэлтгэл ажлыг хуурай, харанхуй газар хадгалдаг.
Хувьцаламж
Нунтаг нь хязгааргүй тавиурын амьдрал, шахмалыг 10 жилийн турш хадгалдаг (хэрэв багц дээрх үйлдвэрлэгчийг өөрөөр заагаагүй бол).
тусгай зөвлөгөө
Одоо фенолфтефенен агуулсан мансууруулах бодис нь эмэнд ховор хэрэглэгддэг. Ихэнх нь ихэвчлэн бусад орчин үеийн, аюулгүй laxatives-т давуу эрх олгодог.
Хүүхдүүд
Бодисыг болгоомжтой байлгана. Хүүхдийн нас, жин, жингээс хамааран тунгийн залруулга хэрэгтэй.
Ах
Хүндео Өөр нас Хүлээн авах үр нөлөө нь 24-72 цагийн дотор явагдана.
Жин хасах зориулалттай
Өнгөрсөн зууны эхэн үед, бодисыг жингээ хасахад ашигладаг байсан. Одоо ижил төстэй нөлөөтэй бусад эмүүд байдаг. Цаг агаарын орчинд олон охидууд төгс төгөлдөр дүр төрхийг буруугаар ашиглах нь зүйтэй. Энэ нь таны эрүүл мэндэд аюултай байж болно.
Агуулсан бэлтгэл (аналог)
ATX 4-р түвшний код:
Экс, purgen, purgen, purgen, purgofen, purgofen, purgilo, fenaloin, laksatol, laksatol, laksatol, laksoyl.
Хаана худалдаж авах вэ
Фенолфтфтеин дахь Phenolphthalein-ийн үнэ нь 1 кг тутамд 1700 рубль юм.
Москвад хэрэгслийг худалдаж авах нь бараг боломжгүй бөгөөд эмийн санд удаан хугацаагаар ашиглагдаагүй байдаг.
Фенолфтенаалины үнэ нь үйлдвэрлэгчээс хамаарч өөр өөр байж болно.
